
分析 反应前,甲容器中A、B的浓度分别为6mol•L-1、3mol•L-1,4min甲容器内的反应达到化学平衡后,A的浓度减少了3.6mol•L-1,B的浓度减少了1.2mol•L-1,浓度变化与化学计量数成正比,则3:b=△c(A):△c(B)=3.6mol/L:1.2mol/L=3:1,则b=1,
(1)根据v=$\frac{△c}{△t}$计算甲容器中反应的平均速率v(B);
(2)根据容器甲和容器乙的体积大小判断反应物浓度大小,浓度越小反应速率越慢,据此判断反应时间;
(3)恒温恒容条件下,达到平衡时丙中B的浓度仍然为0.8mol/L,说明乙和丙为等效平衡,根据等效平衡的知识解答;
(4)根据勒夏特列原理,结合等效平衡规律进行判断;
(5)根据平衡常数的表达式写出反应3A(g)+B(g)?3C(g)+2D(g)的平衡常数,然后计算出此时的浓度商,根据计算结果进行判断.
解答 解:反应前,甲容器中A、B的浓度分别为6mol•L-1、3mol•L-1,4min甲容器内的反应达到化学平衡后,A的浓度减少:6mol•L-1-2.4mol•L-1=3.6 mol•L-1,B的浓度减少:3mol•L-1-1.8mol•L-1=1.2mol•L-1,A、B的浓度变化与化学计量数成正比,则3:b=△c(A):△c(B)=3.6mol/L:1.2mol/L=3:1,则b=1,
(1)甲容器中B的浓度变化为1.2mol•L-1,此时间内平均用B表示的平均反应速率为:v(B)=$\frac{1.2mol/L}{4min}$=0.3 mol/(L•min),
故答案为:0.3 mol/(L•min);
(2)甲容器的体积为1L,乙容器的体积为2L,乙容器的体积大于甲的,浓度小则反应速率小,到达平衡的时间长,所以乙容器中反应达到平衡时所需时间大于4min,
故答案为:大于;
(3)根据等效平衡规律,在恒温恒容下,转化为同一反应方向的物质的物质的量和原来对应相等即可,3molC、2molD完全转化可生成3molA和1molB,则还需3molA和2molB才能与乙为等效平衡,
故答案为:3mol;
(4)由于该反应是体积增大的可逆反应,由于甲的容器体积小,则压强大,平衡向着逆向移动,甲中反应物的转化率小于乙,且达到平衡时甲中各组分浓度都大于乙的,
A.保持温度不变,增大甲容器的体积至2L,则此时甲和乙为等效平衡,甲、乙容器中B的平衡浓度相等,故A正确;
B.保持容器体积不变,使甲容器升高温度,该反应为放热反应,平衡向着逆向移动,甲中B浓度增大,则无法满足甲、乙容器中B的平衡浓度相等,故B错误;
C.保持容器压强和温度都不变,向甲中加入一定量的A气体,由于反应物A的浓度增大,则平衡向着正向移动,甲中B的浓度减小,可能实现甲、乙容器中B的平衡浓度相等,故C正确;
D.保持容器压强和温度都不变,向甲中加入一定量的B气体,达到平衡时甲中B的浓度更大,无法满足甲、乙容器中B的平衡浓度相等,故D错误;
故答案为:AC;
(5)3A(g)+B(g)?3C(g)+2D(g)
反应前(mol/L) 6 3 0 0
浓度变化(mol/L) 3.6 1.2 3.6 2.4
平衡时(mol/L) 2.4 1.8 3.6 2.4
反应3A(g)+B(g)?3C(g)+2D(g)在T℃时的化学平衡常数为:K=$\frac{{c}^{3}(C)•{c}^{2}(D)}{{c}^{3}(A)•c(B)}$=$\frac{3.{6}^{3}×2.{4}^{2}}{2.{4}^{3}×1.8}$=10.8,
该温度下,向体积为1L的密闭容器中通入A、B、C、D气体物质的量分别为3mol、1mol、3mol、2mol,A、B、C、D气体物质的量浓度分别为3mol/L、1mol/L、3mol/L、2mol/L,此时的浓度商为:Qc=$\frac{{c}^{3}(C)•{c}^{2}(D)}{{c}^{3}(A)•c(B)}$=$\frac{{3}^{3}×{2}^{2}}{{3}^{3}×1}$=4<K=10.8,说明反应物浓度偏大、生成物浓度偏小,平衡向正反应方向进行,
故答案为:向正反应方向进行.
点评 本题考查较为综合,涉及化学平衡常数的计算、化学平衡的影响因素、化学反应速率的计算等知识,题目难度中等,注意掌握化学平衡常数的影响因素及计算方法,明确化学反应速率与化学计量数的关系,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | AI溶解于氢氧化钠溶液中 | B. | Na与水反应 | ||
| C. | Na2O2与水反应 | D. | Fe与水蒸气在高温下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑦ | B. | ②④⑥ | C. | ①⑥⑦ | D. | ①②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金中铁的质量为5.4 g | |
| B. | 合金与稀硫酸反应共生成0.45 mol H2 | |
| C. | 该合金与足量氢氧化钠溶液反应,转移的电子数为0.3NA | |
| D. | 所加的稀硫酸中含0.6 mol H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
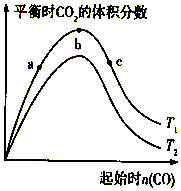 燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注.一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol.保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):下列有关说法正确的是( )
燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注.一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol.保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):下列有关说法正确的是( )| A. | T1比T2高 | |
| B. | b点SO2转化率最高 | |
| C. | b点后曲线下降是因CO体积分数升高 | |
| D. | 减小压强可提高CO、SO2转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)若向Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,试从平衡的角度解释沉淀转化的原因:氢氧化镁浊液中存在沉淀溶解平衡:Mg(OH)2?Mg2++2OH-,由于KSP[Fe(OH)3]<KSP[Mg(OH)2],所以当加入Fe3+后,会和OH-反应生成更难溶的氢氧化铁沉淀,使得上述平衡正向移动,最有氢氧化镁全部转化为红褐色的氢氧化铁沉淀
(1)若向Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,试从平衡的角度解释沉淀转化的原因:氢氧化镁浊液中存在沉淀溶解平衡:Mg(OH)2?Mg2++2OH-,由于KSP[Fe(OH)3]<KSP[Mg(OH)2],所以当加入Fe3+后,会和OH-反应生成更难溶的氢氧化铁沉淀,使得上述平衡正向移动,最有氢氧化镁全部转化为红褐色的氢氧化铁沉淀查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2mol/(L•min) | B. | 1mol/(L•min) | C. | 0.6mol/(L•min) | D. | 0.4mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com