
中国是世界上最早利用天然气作燃料的国家.天然气的主要成分是( )
|
| A. | CH4 | B. | CO | C. | H2 | D. | CO2 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
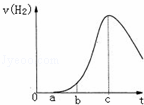
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L﹣1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图的坐标曲线来表示,下列推论错误的是( )
|
| A. | t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
|
| B. | t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
|
| C. | t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
|
| D. | t=c时反应处平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,我国拥有完全自主产权的氢氧燃料电池车已经在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是( )
A.负极反应式为2H2+4OH--4e-====4H2O
B.工作一段时间后,电解液中的KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2====2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
一种光化学电池的结构如图所示,电池总反应为AgCl(s)+
Cu+(aq)====Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是 ( )
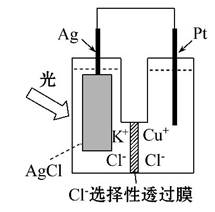
A.Cl-由负极迁移到正极
B.负极上物质发生还原反应
C.Cu+在负极发生氧化反应
D.生成108 g银,转移电子个数为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是( )
|
| A. | 氯化钠的电子式:Na: |
|
| B. | 乙烯的结构简式:C2H4 |
|
| C. | 硅的原子结构示意图: |
|
| D. | 硫酸的电离方程式:H2SO4=H22++SO42 |
查看答案和解析>>
科目:高中化学 来源: 题型:
N2+3H2 2NH3是目前工业上合成氨的反应,下列关于该反应的说法正确的是( )
2NH3是目前工业上合成氨的反应,下列关于该反应的说法正确的是( )
|
| A. | 增加N2的浓度能加快反应速率 |
|
| B. | 降低体系温度能加快反应速率 |
|
| C. | 使用催化剂不影响反应速率 |
|
| D. | 若反应在密闭容器中进行,N2和H2能100%转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源.
(1)在汽车尾气系统中安装催化转换器,可有效减少尾气中的CO、NOx 和碳氢化合物等废气.
已知:N2(g)+O2(g)=2NO(g)△H1=+180kJ/mol
CO(g)+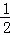 O2(g)=CO2(g)△H2=﹣283kJ/mol
O2(g)=CO2(g)△H2=﹣283kJ/mol
2NO(g)+2CO(g)=2CO2(g)+N2(g)△H3则△H3= kJ•mol﹣1.
(2)气缸中生成NO的反应为:N2(g)+O2(g)═2NO(g)△H>0
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因是 .
②1mol空气中含有0.8molN2和0.2molO2,1300℃时在含1mol空气的密闭容器内反应达到平衡,测得NO为8×10﹣4mol.计算该温度下的平衡常数K≈ .
(3)尾气中的CO主要来自于汽油不完全燃烧.
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)△H=+221kJ•mol﹣1,简述该设想能否实现的依据:
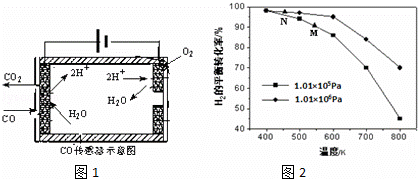
②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用如图1简单表示,则阳极发生的电极反应为 .
(4)汽车尾气中的CO可转化为甲烷,方程式为CO(g)+3H2(g)⇌CH4(g)+H2O(g).其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图2所示.
①该反应的△H 0(填“<”、“=”或“>”).
②实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com