
用11.5g金属钠放入水中,要使100个水分子溶有1个钠离子,则需加水 g。
909g
【解析】
利用n=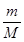 计算Na的物质的量,由Na原子守恒可知,n(Na)=n(Na+),再利用100个水分子中溶有1个钠离子来列式计算出水的物质的量及其质量即可。
计算Na的物质的量,由Na原子守恒可知,n(Na)=n(Na+),再利用100个水分子中溶有1个钠离子来列式计算出水的物质的量及其质量即可。
n(Na)=n(Na+)=11.5g÷23g/mol=0.5mol
根据方程式2Na+2H2O=2NaOH+H2↑可知参加反应的水的物质的量是0.5mol
由100个水分子中溶有1个钠离子可知,反应后水的物质的量是0.5mol×100=50mol,所以共计需要水的物质的量是50mol+0.5mol=50.5mol,质量是50.5mol×18g/mol=909g。
考点:考查钠与水反应的有关计算
点评:该题是中等难度的试题,主要是考查学生对钠与水原理以及物质的量计算的了解掌握情况,有利于培养学生的逻辑推理能力和规范答题能力。明确质量、物质的量的关系及信息中水分子与钠离子的关系即可解答。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com