
分析 ①PM2.5”是指大气层中直径≥2.5μm的颗粒物,能被肺吸收并进入血液,对人体危害很大,是形成雾霾的主要污染物;
②劣质胶合板释放的主要污染物是甲醛,释放后造成室内污染;
③明矾溶于水生成氢氧化铝胶体;使用漂白粉或漂白精片进行杀菌消毒,反应生成HClO,具有强氧化性.
解答 解:①导致雾霾形成的主要污染物是pM2.5,故选B,故答案为:B;
②甲醛是劣质胶合板释放的主要污染物,造成室内污染,故选C,故答案为:C;
③明矾可用于净水,是因为明矾溶于水生成的胶状物质可以吸附悬浮于水中的杂质,使之从水中沉降出来;使用漂白粉或漂白精片进行杀菌消毒,反应生成HClO,具有强氧化性,该反应为Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,
故答案为:A;Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO.
点评 本题主要考查了根据方程式计算、方程式书写以及漂白原理等、常见的污染物,与生产生活密切相关,题目难度不大,注意知识的积累.


科目:高中化学 来源: 题型:实验题
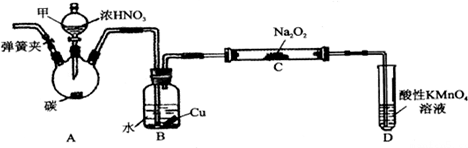
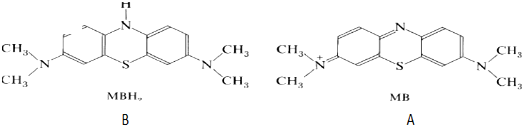
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
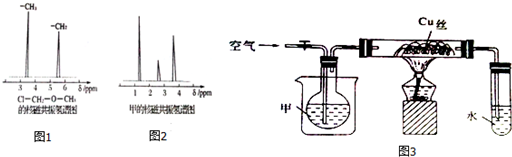
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量多 | |
| B. | 热化学方程式C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(g)△H=-1256 kJ•mol-1,可知乙炔的燃烧热为1256 kJ•mol-1 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| D. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出234kJ热量 | |
| B. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| C. | 若X表示反应时间,则Y表示的可能是混合气体的密度 | |
| D. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=-0.33 kJ/mol | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3<0,单斜硫比正交硫稳定 | |
| D. | △H3>0,单斜硫比正交硫稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/°C | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
| A. | 若500℃时进行反应①,则CO2转化率为50% | |
| B. | 900℃进行反应③H2(g)+CO2(g)?H2O(g)+CO(g),其平衡常数K3为=1.50 | |
| C. | 反应①的焓变△H>0,反应②的焓变△H<0 | |
| D. | 反应①平衡体系中通入CO2,在温度不变的条件下,平衡正向移动,达到新平衡时CO2的转化率比原平衡小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取操作震荡时,用右手压住分液漏斗口部,用左手握住活塞部分 | |
| B. | 蒸馏操作时,冷却水应从冷凝管的下口进,上口出 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作选择有机萃取剂时,萃取剂的密度必须比水大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com