
| A. | CO2的电子式: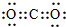 | B. | 乙炔的结构式:H-C≡C-H | ||
| C. | CH4的比例模型: | D. | Cl-的结构示意图: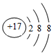 |
分析 A.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子;
B.乙炔分子含有2个C-H,1个C≡C;
C.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型;
D.氯离子核内有17个质子,核外有18个电子,分布在3个电子层上,分别容纳2,8,8个电子.
解答 解:A.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故A错误;
,故A错误;
B.乙炔为共价化合物,乙炔分子含有2个C-H,1个C≡C,乙炔的结构式:H-C≡C-H,故B正确;
C.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型,则CH4分子的比例模型为 ,故C正确;
,故C正确;
D..氯离子核内有17个质子,核外有18个电子,分布在3个电子层上,分别容纳2,8,8个电子,Cl-的结构示意图: ,故D正确;
,故D正确;
故选:A.
点评 本题考查常用化学用语的书写,掌握电子式、结构式、比例模型、原子结构示意图等常用化学用语的书写方法是解题管就,注意比例模型突出的是原子之间相等大小以及原子的大致连接顺序、空间结构,不能体现原子之间的成键的情况,题目难度中等.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:解答题
 ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为: +(CH3CO)2O$→_{85-90℃}^{浓硫酸}$
+(CH3CO)2O$→_{85-90℃}^{浓硫酸}$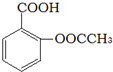 +CH3COOH操作流程如下:
+CH3COOH操作流程如下:
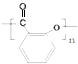 .
.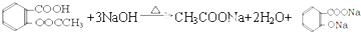 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族元素的原子半径越大,熔点越高 | |
| B. | 在元素周期表中,s区,d区和ds区的元素都是金属 | |
| C. | 石墨晶体中的作用力有共价键、金属键两种,是一种混合晶体 | |
| D. | 在晶体中只要有阴离子就一定有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、K+、SO42-、Br- | B. | K+、Na+、AlO2-、Cl- | ||
| C. | Fe3+、K+、SO42-、NO3- | D. | K+、Na+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化亚铁和稀盐酸反应:FeS+2H+=Fe2++H2S↑ | |
| B. | 次氯酸钠溶液中通入少量SO2反应:SO2+H2O+ClO-=SO42-+Cl-+2H+ | |
| C. | 过氧化钠加入足量稀硫酸反应:2Na2O2+4H+═4Na++O2↑+2H2O | |
| D. | 铜粉中加入溴化铁溶液反应:2Fe3++Cu=2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 用激光笔分别照射蛋白质溶液、硅酸溶胶 | 将二者区别开 |
| B | 将C2H5OH与浓H2SO4在蒸馏烧瓶中混合后加热至 170℃,烧瓶内逸出的物质通入到酸性KMnO4溶液中 | 检验有无乙烯生成 |
| C | 将Al(OH)3置于适量0.2mol•L-1 FeCl3溶液中,-段时间后可得到红褐色固体 | 溶度积:Ksp[AL(OH)3]>Ksp[Fe(OH)3] |
| D | 向蔗糖溶液中加入适量稀硫酸,水浴加热几分钟,然后加入新制的银氨溶液,并水浴加热 | 检验蔗糖的水解产物是否具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:5 | B. | 2:7 | C. | 2:5 | D. | 2:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com