
����Ŀ����֪��ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ���������������ԭ������ش��������⣺
��1�����淴ӦFeO(s)��CO(g)![]() Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
T/K | 938 | 1 100 |
K | 0.68 | 0.40 |
���÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬���������¶ȣ���������ƽ����Է�������_____�����뺤�������������ܶ�____(��������������С������������)��
��2��830������ӦCO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)��ƽ�ⳣ��K=1����2L���ݷ�Ӧ���з���������Ӧ���ֱ����3mol CO2��,2mol H2��1mol CH3OH��4mol H2O����Ӧ��__������С�������/�ң�
CH3OH(g)��H2O(g)��ƽ�ⳣ��K=1����2L���ݷ�Ӧ���з���������Ӧ���ֱ����3mol CO2��,2mol H2��1mol CH3OH��4mol H2O����Ӧ��__������С�������/�ң�
��3�������£�Ũ�Ⱦ�Ϊ0.1 mol��L��1������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
����������Һ�е������ӣ��������������ǿ����______��
�ڸ��ݱ��������жϣ�Ũ�Ⱦ�Ϊ0.01 mol��L-1�������������ʵ���Һ�У�������ǿ����____��������Һ�ֱ�ϡ��100����pH�仯��С����_____(����)��
A��HCN B��HClO C��H2CO3 D��CH3COOH
�۾��ϱ����ݣ������ж����з�Ӧ���ܳ�������___(����)��
A��CH3COOH+Na2CO3=NaHCO3+CH3COONa
B��CH3COOH+NaCN=CH3COONa+HCN
C��CO2+H2O+2NaClO=Na2CO3
��Ҫ������ˮ��HClO��Ũ�ȣ�������ˮ�м���������̼������Һ����Ӧ�����ӷ���ʽΪ__________��
���𰸡���С ���� �� CO32- D A C 2Cl2+CO32-+H2O=CO2��+2Cl-+2HClO
��������
��1�����ݱ����е����ݣ���ѧƽ�ⳣ�������¶ȵ����߶���С��˵���÷�Ӧ������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ���淴Ӧ������У���������ƽ��Ħ��������С�����뺤�������������������ӣ�����Ϊ����װ�ã������������ܶ�����
��2��CO2��H2��CH3OH��H2O��Ũ�ȷֱ���1.5mol��L-1��1mol��L-1��0.5mol��L-1��2mol��L-1��Qc=![]() =
=![]() ��1����Ӧ���ҽ��У�
��1����Ӧ���ҽ��У�
��3������������ˮ���С�Խ��Խˮ�⡱��pHԽ��˵�����������ˮ��̶�Խ��Խ�����H�������ݱ������ݣ��Ƴ����H������H����ǿ����CO32����
�ڸ��ݱ����е����ݣ���������ˮ���С�Խ��Խˮ�⡱���Ƴ������H�������Ĵ�С��CH3COOH��H2CO3��HClO��HCN��HCO3-�����Ũ�Ⱦ�Ϊ0.01mol��L-1��������Һ�У�������ǿ����CH3COOH����ͬŨ�ȵIJ�ͬ��ϡ����ͬ�ı������������Խ���������pH�仯ԽС����������������HCN����pH�仯��С��HCN��
�����ø��ݱ����е����ݣ���������ˮ���С�Խ��Խˮ�⡱���Ƴ������H�������Ĵ�С��CH3COOH��H2CO3��HClO��HCN��HCO3-��
A��CH3COOH������Na2CO3����������CH3COOH+Na2CO3=NaHCO3+CH3COONa����A������
B����������ǿ����ȡ������������CH3COOH+NaCN=CH3COONa+HCN����B������
C�����������������Ƴ�CO2+H2O+NaClO=NaHCO3+HClO����C��������
��ѡC��
��������H2O����Cl2+H2O![]() HCl+HClO����������Na2CO3��Ӧ����Ϊ����������̼������Һ�����ֻ����HCl+Na2CO3=NaHCO3+NaCl������Ӧ�����ӷ���ʽΪ2Cl2+2CO32-+H2O=CO2��+2Cl-+2HClO��
HCl+HClO����������Na2CO3��Ӧ����Ϊ����������̼������Һ�����ֻ����HCl+Na2CO3=NaHCO3+NaCl������Ӧ�����ӷ���ʽΪ2Cl2+2CO32-+H2O=CO2��+2Cl-+2HClO��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������
A.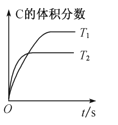 ��ʾ����ͬ���ܱ������У���ӦA(g)+B(g)
��ʾ����ͬ���ܱ������У���ӦA(g)+B(g) ![]() 2C(g)��һ���¶���C�����������ʱ��ı仯�������÷�Ӧ����H>0
2C(g)��һ���¶���C�����������ʱ��ı仯�������÷�Ӧ����H>0
B. ��ʾ0.1000 mol��L-1NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L-1HX��Һ�ĵζ����ߣ���HX����Ϊ����
��ʾ0.1000 mol��L-1NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L-1HX��Һ�ĵζ����ߣ���HX����Ϊ����
C.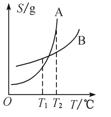 ��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������T1 ��ʱA��B�ı�����Һ�ֱ�������T2 �棬�����ʵ�����������w(A)>w(B)
��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������T1 ��ʱA��B�ı�����Һ�ֱ�������T2 �棬�����ʵ�����������w(A)>w(B)
D.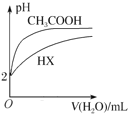 ��ʾ25 ��ʱ���ֱ��ˮϡ�������Ϊ100 mL pH=2��CH3COOH��Һ��HX��Һ����25 ��ʱ����ƽ�ⳣ����Ka(HX)<Ka(CH3COOH)
��ʾ25 ��ʱ���ֱ��ˮϡ�������Ϊ100 mL pH=2��CH3COOH��Һ��HX��Һ����25 ��ʱ����ƽ�ⳣ����Ka(HX)<Ka(CH3COOH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ȼ��֮һ�������������泥�NH4ClO4���Ĺ��������ȼʱ�����۱���������������������立�Ӧ��2NH4ClO4�TN2��+4H2O+Cl2��+2O2������Ӧ�ų������ȡ�
��1���÷�Ӧ�б�������Ԫ����___��___��
��2�����������뻹ԭ���������֮��Ϊ___��
��3���÷�Ӧ�������ɱ����2.24LCl2ʱ������ת����Ϊ___��
��4�������ɵ�ˮ�ڸ�����ҲΪ��̬�����������ƽ��Ħ������Ϊ__g/mol(С�������һλ)��
��5���������(K2FeO4)��һ��ǿ��������������ˮ������Ϊˮ��������������ز��ϡ�FeCl3��KClO��ǿ���������·�Ӧ����ȡK2FeO4���䷴Ӧ�����ӷ���ʽΪ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��Ϊ�������������������������ʵ�ת�����̻ش�������⣺
Fe![]() A
A![]() B
B![]() C
C
��1����Ӧ������������������ԭ��Ӧ����________________������ţ���
��2����B����Һ�е��뼸��KSCN��Һ�ɹ۲쵽��������__________��
��3����Ӧ�������ӷ���ʽΪ _____________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��������ֵĵڶ���������ѧ������Ԫ�ء��ش��������⣺
��1������Ԫ�����ڱ���λ��Ϊ______________��HF�ķе��HI_________����������������������ԭ����_____________________________
��2����Ȼ���еĵ��е���NaIO3��̬��������ʯ(NaNO3)�У�����ʯĸҺ�м���NaHSO3�����Ƶ�I2����д��NaIO3��Һ��NaHSO3��Һ��Ӧ�����ӷ���ʽ___________________��
II��2019���п�ѧ�ҷ����ڡ���Ȼ����ѧ��־�ϵ��о���Ϊ��ϸ�����鳤�ද����Ԫ������ս�����ִ���һ�����������ء���������ѧ��֪ʶ�ش��������⣺
��1������26��Ԫ�أ���ԭ�ӽṹʾ��ͼΪ_______________________
��2��д�������������Ӵ�������ɫ�����з����Ļ�ѧ����ʽ_________________________
��3��Na2FeO4������ˮ����������������ˮ�����е����ú�ԭ��_______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��800��ʱ����2L���ܱ������з�����Ӧ��2NO(g)+O2(g)![]() 2NO2��n(NO)��ʱ��ı仯���±���ʾ��
2NO2��n(NO)��ʱ��ı仯���±���ʾ��
ʱ���Ms | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)�Mmol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����0��3s�ڣ���NO��ʾ��ƽ����Ӧ������(NO)��_____________��
��2��ͼ�б�ʾNOŨ�ȱ仯��������_______(����ĸ����)��
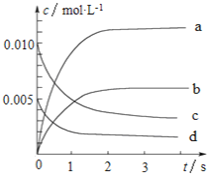
��3����ƽ��ʱNO��ת����Ϊ________��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬����_________(�����)��
A������������ɫ���ֲ���
B�����������ܶȱ��ֲ���
C������ (NO2)��2���� (O2)
D����������ƽ����Է����������ֲ���
��5�������µ�850�棬��ƽ���n(NO)��n(NO2)����Ӧ��________(��������Ӧ�����������淴Ӧ������)�ƶ���
��6������һ��������0.2molNO������������Ӧ����ƽ��ʱ��÷ų�������ΪakJ����ʱNOת����Ϊ80%����2molNO������ȫ��Ӧ�ų�������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 18g����(��ND2)�к��еĵ�����Ϊ10NA
B. һ��������������22.4L(��״��)Cl2�ڹ��������·���ȡ����Ӧ���γ�C��Cl������ĿΪ2NA
C. �ö��Ե缫���100mL0.1mol��L��1��CuSO4��Һ��������������������ͬ�����µ����������ʱ����·��ת�Ƶ�����Ϊ0.04NA
D. n(H2SO3)��n(HSO3��)֮��Ϊ1mol��KHSO3��Һ�У����е�K+��ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϲ������Ը�Ũ�Ⱥ����ˮ(����Ҫ��������H3AsO3��ʽ����)��ȡ��ҩҩ��As2O3�������������£�
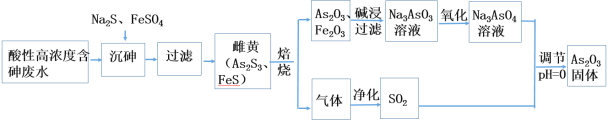
�ش��������⣺
��1����֪��Ԫ����Nͬһ���壬ԭ�ӱ�Nԭ�Ӷ��������Ӳ㣬����Ԫ�ص�ԭ������Ϊ________�������顱������Na2S�ĵ���ʽΪ_____________��
��2����֪��As2S3�������S2-�������·�Ӧ��As2S3(s)+3S2-(aq) ![]() 2AsS33- �������顱��FeSO4��������___________________________��
2AsS33- �������顱��FeSO4��������___________________________��
��3�������ա�����������������ԭ�����ɵ������������л���������������֤���������������ڵ��Լ���_________________________________��(д����)
��4������pH=0ʱ����Na3AsO4�Ʊ�As2O3�����ӷ���ʽΪ��_______________��
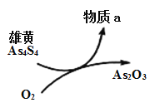
��5��һ�������£����ۻ�(As4S4)�Ʊ�As2O3��ת����ϵ��ͼ��ʾ������Ӧ�У�1molAs4S4(����AsԪ�صĻ��ϼ�Ϊ+2��)�μӷ�Ӧʱ��ת��28mole-��������aΪ___________��(�ѧʽ)
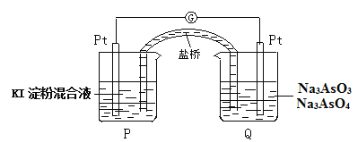
��6��ijԭ���װ����ͼ������ܷ�ӦΪ��AsO43-+2I-+H2O![]() AsO33-+I2+2OH-����P������Һ����ɫ�����ɫʱ�������ϵĵ缫��ӦʽΪ____________________________��һ��ʱ��������ָ�벻����ƫת����ʹָ��ƫת��������ʼʱ�෴���ɲ�ȡ�Ĵ�ʩ��____________(��һ��)��
AsO33-+I2+2OH-����P������Һ����ɫ�����ɫʱ�������ϵĵ缫��ӦʽΪ____________________________��һ��ʱ��������ָ�벻����ƫת����ʹָ��ƫת��������ʼʱ�෴���ɲ�ȡ�Ĵ�ʩ��____________(��һ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10-5 | K1��4.3��10-7 K2��5.6��10-11` | 3.0��10-8 |
��ش��������⣺
��1���г�CH3COONa��ˮ��ƽ�ⳣ��Kh�ļ���ʽ��_________��
��2�����ʵ���Ũ����ͬ��������Һ��a.CH3COONa b��NaHCO3 c��NaClO
������Һ��pH��С�������е�˳����___<___< ____(�ñ����д)��
��3��д����NaClO��Һ��ͨ������CO2�Ļ�ѧ����ʽ________��
��.��4��̼������Һ�ʼ��Ե�ԭ���ǣ�_____________����д�����ӷ���ʽ����0.01mol/L Na2CO3��Һ��pH___0.1mol/LNa2CO3��Һ��pH������������������������=����
��5��Ũ�Ⱦ�Ϊ0.1mol/L�Ģ�CH3COONa��Һ��NH4Cl��Һ��ϡHCl��Na2SO4��Һ��pH�ɴ�С������˳��Ϊ_______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com