
【题目】煤燃烧排放的烟气含有SO2和NOx , 形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)SO2分子的空间构型为 .
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10﹣3molL﹣1 . 反应一段时间后溶液中离子浓度的分析结果如表.
离子 | SO42﹣ | SO32﹣ | NO3﹣ | NO2﹣ | Cl﹣ |
c/(molL﹣1) | 8.35×10﹣4 | 6.87×10﹣6 | 1.5×10﹣4 | 1.2×10﹣5 | 3.4×10﹣3 |
①写出NaClO2溶液脱硫过程中主要反应的离子方程式 . 增加压强,SO2的转化率(填“提高”“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐 (填“提高”“不变”或“降低”).
③由实验结果可知,脱硫反应速率脱硝反应速率(填“大于”或“小于”).原因是除了SO2和NO在烟气中的初始浓度不同,还可能是 .
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压Pa如图所示. 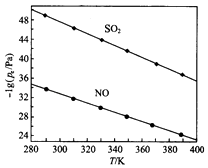
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均(填“增大”“不变”或“减小”).
②反应ClO2﹣+2SO32﹣=2SO42﹣+Cl﹣的平衡常数K表达式为
(4)如果采用NaClO、Ca(ClO)2替代NaClO2 , 也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是 .
【答案】
(1)V形
(2)3ClO2﹣+4NO+4OH﹣=4NO3﹣+3Cl﹣+2H2O;提高;降低;大于; NO溶解度较低或脱硝反应活化能较高
(3)减小; 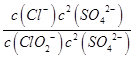
(4)形成CaSO4沉淀,降低硫酸根离子浓度,反应平衡向产物方向移动,SO2转化率提高
【解析】解:(1)SO2中S原子价层电子对=2+ ![]() (6﹣2×2)=3,所以采取sp2杂化方式,该分子中含有一个孤电子对,所以其空间构型是V形,
(6﹣2×2)=3,所以采取sp2杂化方式,该分子中含有一个孤电子对,所以其空间构型是V形,
所以答案是:V形;(2)①亚氯酸钠具有氧化性,且NaClO2溶液呈碱性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2﹣+4NO+4OH﹣=4NO3﹣+3Cl﹣+2H2O;正反应是体积减小的,则增加压强,NO的转化率提高,
所以答案是:3ClO2﹣+4NO+4OH﹣=4NO3﹣+3Cl﹣+2H2O;提高;
②根据反应的方程式3ClO2﹣+4NO+4OH﹣=4NO3﹣+3Cl﹣+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低,
所以答案是:降低;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高,
所以答案是:大于;NO溶解度较低或脱硝反应活化能较高;(3)①由图分析可知,根据反应3ClO2﹣+4NO+4OH﹣=4NO3﹣+3Cl﹣+2H2O,NO的平衡分压的负对数随温度的升高而减小,则说明温度越高,NO的平衡分压越大,NO的含量越高,故升高温度,平衡向逆反应方向进行,平衡常数减小,所以答案是:减小;
②根据反应的方程式ClO2﹣+2SO32﹣═2SO42﹣+Cl﹣可知平衡常数K表达式为K= ![]() ,所以答案是:
,所以答案是: ![]() ;(4)如果采用NaClO、Ca(ClO)2替代NaClO2,生成硫酸钙沉淀,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果好,
;(4)如果采用NaClO、Ca(ClO)2替代NaClO2,生成硫酸钙沉淀,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果好,
所以答案是:形成CaSO4沉淀,降低硫酸根离子浓度,反应平衡向产物方向移动,SO2转化率提高;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃.
(1)基态锌原子的价电子排布式是 .
(2)根据元素周期律,电负性SeS,第一电离能SeAs(填“>”或“<”).
(3)H2Se的分子构型是 , 其中Se的杂化轨道类型是 .
(4)H2O的沸点(填“>”或“<”)H2Se的沸点,其原因是: .
(5)晶体Zn为六方最密堆积,其配位数是 .
(6)在硒化锌ZnSe晶胞中,Se2﹣离子作面心立方最密堆积,且Se2﹣与Se2﹣之间的最短距离为a nm,则晶胞边长为 nm.
(7)假设阿伏伽德罗常数值为NA , 则144g 硒化锌ZnSe晶体中的晶胞数是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据20℃时某些物质的溶解度(g)数据:
CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
1.4×10﹣3 | 2.55×10﹣2 | 9×10﹣4 | 1.1×10﹣2 |
下列说法不正确的是( )
A.硫酸钙悬浊液中存在CaSO4(s)Ca2+(aq)+SO42﹣(aq)
B.用Na2CO3溶液浸泡锅炉中的水垢,可将水垢中的CaSO4转化为CaCO3
C.向Mg(OH)2悬浊液中滴加FeCl3 , 沉淀变为红褐色,说明溶解度Fe(OH)3<Mg(OH)2
D.向2ml饱和MgCl2 溶液中先后滴加0.1mol/L的Na2CO3、NaOH溶液各2滴,产生的白色沉淀为Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬铁矿[Fe(CrO2)2]为原料可制备K2Cr2O7和金属铬。实验流程如下:
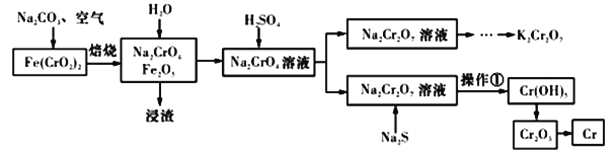
已知:2CrO42-+2H+=Cr2O72-+H2O。pH<3.0,CrO42-含量极小。
(1)写出铬铁矿焙烧转化为Na2CrO4的化学反应方程式:_____________________。焙烧时不能使用陶瓷容器的原因是________________________________________。
(2)判断加入稀硫酸的量已经足量的标准是_______________________________________。
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是________________________________。
(4)Na2S的作用是调节溶液的酸碱度和_____________________。
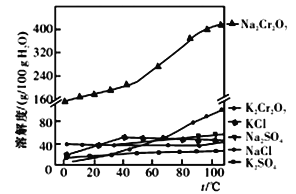
(5)Fe3+在pH为3.7时可完全转化为Fe(OH)3。在上述流程中所得Na2Cr2O7溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7溶液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸溶液、NaOH溶液、KCl固体、蒸馏水):
步骤①除杂质:__________________________________________________________________;
步骤②制备K2Cr2O7固体:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.棉花和蚕丝的主要成分是纤维素
B.蛋白质在一定条件下可以发生水解生成葡萄糖
C.煤的气化是在高温下煤和水蒸汽作用转化为可燃性气体的过程
D.油脂的主要成分是高级脂肪酸甘油酯,在碱性条件下水解可以得到高级脂肪酸和甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应适用于工业生产的是
A.电解熔融氯化铝可得到金属铝B.光照氯气和氢气的混合物生产盐酸
C.氯气与石灰乳作用制漂白粉D.二氧化锰和浓盐酸共热,制取氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大约占细胞鲜重总量97%的元素主要是
A.C、H、O、N、P、SB. C、H、O、N、P、K
C.C、H、O、N、Cu、MgD.N、P、S、K、Ca、Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com