
 FeO+CO2↑+CO↑+2H2O。甲同学欲检验晶体分解生成的CO2、CO和水蒸气,设计了如下实验装置(央持仪器已略去):
FeO+CO2↑+CO↑+2H2O。甲同学欲检验晶体分解生成的CO2、CO和水蒸气,设计了如下实验装置(央持仪器已略去): 
 Fe+CO2,请你设汁一个简单的化学实验验证该结论(写出实验操作步骤、现象与结论):__________________________。
Fe+CO2,请你设汁一个简单的化学实验验证该结论(写出实验操作步骤、现象与结论):__________________________。  名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解

 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


c[Cu(NH3
| ||
| c(Cu2+)?c4(NH3) |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.
Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤(不要求具体的操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, |
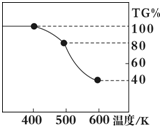
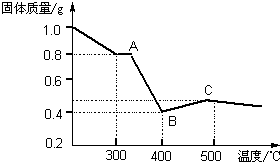 [定量研究]课题组在文献中查阅到,FeC2O4?2H2O受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,FeC2O4?2H2O晶体受热分解的化学方程式为:
[定量研究]课题组在文献中查阅到,FeC2O4?2H2O受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,FeC2O4?2H2O晶体受热分解的化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com