
【题目】下列粒子中,半径最小的是( )
A.Na+B.NaC.Mg2+D.Cl-
科目:高中化学 来源: 题型:
【题目】2-甲基-1,3-丁二烯是一种重要的化工原料。可以发生以下反应。已知:
![]() 。
。
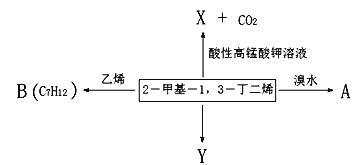
请回答下列问题:
(1)2-甲基-1,3-丁二烯与溴水发生加成反应。
①完全加成所得有机产物的名称____________;
②发生1,2-加成所得有机产物的结构简式为_______________________;
③发生1,4-加成反应的化学方程式为_______________________________________。
(2)B为含有六元环的有机物,写出2-甲基-1,3-丁二烯与乙烯反应的化学方程式______________。
(3)Y(![]() )是天然橡胶的主要成分。能发生的反应有_________(填标号)。
)是天然橡胶的主要成分。能发生的反应有_________(填标号)。
A.加成反应 B.氧化反应 C.消去反应 D.酯化反应
(4)X的分子式为C3H4O3,其结构简式为_________________;X与乙醇发生酯化反应的化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.酯化反应也属于加成反应
B.酯化反应中羧酸脱去羧基中的羟基,醇脱去羟基中的氢原子生成水
C.浓硫酸在酯化反应中只起催化剂的作用
D.欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀有金属铟由于其良好的性能常用于生产液晶显示器和平板屏幕,下图是铟元素的相关信息,下列有关铟的说法错误的是
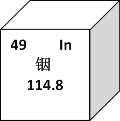
A. 115In原子核内有66个中子
B. 115In原子核外有49个电子
C. 115In、113In互为同位素
D. 115In、113In的化学性质有较大的不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.10 mol/L甲胺的溶液中滴加0.10 mol/L盐酸时混合溶液的pH与相关微粒的浓度关系如图所示。已知:甲胺(CH3NH2)类似于氨,但碱性稍强于氨。下列说法不正确的是

A. 甲胺在水中的电离方程式CH3NH2+H2O![]() CH3NH3++OH—
CH3NH3++OH—
B. b点对应的加入盐酸的体积小于20mL
C. 将等物质的量的CH3NH2和CH3NH3Cl一起溶于蒸馏水,得到对应a点的溶液
D. 常温下,甲胺的电离常数为Kb,则pKb=—lgKb=3.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废料和废水的处理离不开化学。
I. 某工业废料含SiO2、FeS和CuS等物质,采用如下实验方案进行回收利用。请回答下列问题:
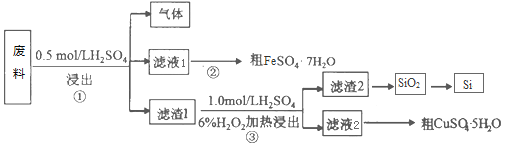
(1)已知步骤①中发生的化学反应为非氧化还原反应,写出产生气体的电子式_______,该气体可用足量的NaOH溶液吸收,该反应的离子方程式是_______________________________
(2)Si原子在周期表中的位置____________,写出晶体Si的一种主要用途___________。步骤②的操作依次为____________________、过滤、洗涤、干燥。滤渣2的主要成分是SiO2和S,写出步骤③涉及的化学方程式_________________________________。
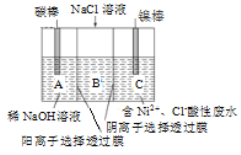
II.用一种阴、阳离子双隔膜三室电解槽处理含镍酸性废水并获得金属镍的模拟装置如图。
镍棒与外接电源____极相连。A极区电极反应式是__________________________。 电解一段时间后,B中NaCl溶液的浓度_________填“增大”、“减少”);若将图中阳离子膜去掉,将A、B两室合并,则A极区电极产物是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是
A. SO2 + 2NaOH = Na2SO3 + H2O B. 2CuO + C![]() 2Cu + CO2↑
2Cu + CO2↑
C. 2FeCl3 + Fe = 3FeCl2 D. Zn+2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C![]() 2AlN+3CO合成。下列叙述不正确的是
2AlN+3CO合成。下列叙述不正确的是
A. 上述反应中, C是还原剂,AlN是还原产物
B. 上述反应中,每生成1 mol AlN需转移3 mol电子
C. AlN中氮元素的化合价为-3
D. AlN的摩尔质量为41
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com