
| m |
| M |
| n |
| V |
| 34.2g |
| 342g/mol |
| 0.3mol |
| 0.25L |


科目:高中化学 来源: 题型:
A、CH4 ( g )+
| ||
B、S ( s )+
| ||
| C、C6H12O6 ( s )+6O2 ( g )=6CO2 (g)+6H2O ( l )△H3 | ||
| D、2CO ( g )+O2( g )=2CO2 ( g )△H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2溶液中加入少量NaHCO3溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
| B、过量氯气通入FeBr2溶液中:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| C、二氧化硫气体通入碘水中:SO2+I2+2H2O=2H++SO42-+2HI |
| D、向明矾溶液中加入Ba(OH)2溶液至沉淀质量最大:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的物质的量浓度变小 |
| B、溶液中溶质的质量不变 |
| C、溶液中溶质的质量分数变小 |
| D、溶液中溶质的物质的量变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
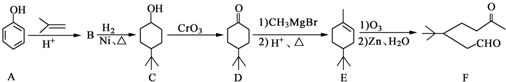
 )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
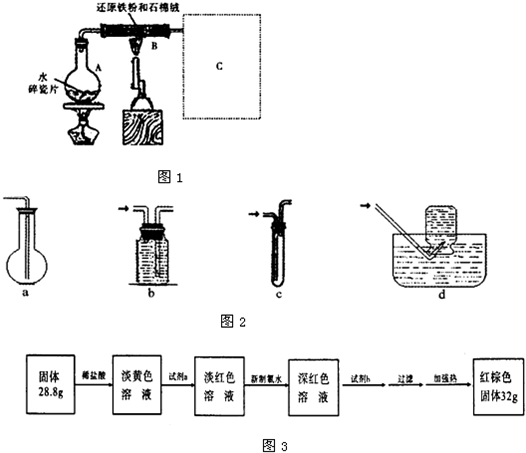
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com