
”¾ĢāÄæ”æijĶ¬Ń§ÓĆĻĀĶ¼ĖłŹ¾µÄ×°ÖĆ¼°Ņ©Ę·½ųŠŠ±Č½ĻĖįŠŌĒæČõµÄŹµŃ飬Ņ»¶ĪŹ±¼äŗóŹŌ¹Ü¢ŚÖŠÓŠ½ŗ¶³×“ĪļÖŹÉś³É”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
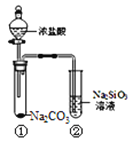
A. ÓĆ“ųÓŠ²£Į§ČūµÄŹŌ¼ĮĘæŹ¢×°Na2SiO3ČÜŅŗ
B. ŹŌ¹Ü¢ŁÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗNa2CO3+ 2H+ = 2Na+ + CO2”ü+ H2O
C. øĆŹµŃéæÉŅŌÖ¤Ć÷ĖįŠŌ£ŗŃĪĖį£¾Ģ¼Ėį£¾¹čĖį
D. Čō½«ŃĪĖį»»³ÉĮņĖį£¬ÄÜÖ¤Ć÷ĖįŠŌ£ŗĮņĖį£¾Ģ¼Ėį£¾¹čĖį
”¾“š°ø”æD
”¾½āĪö”æA”¢Na2SiO3ŹĒ³£¼ūµÄ²£Į§Õ³ŗĻ¼Į,»įŹ¹²£Į§ČūÕ³×”,°Ī¶¼°Ī²»ĻĀĄ“£¬²»ÄÜÓĆ“ųÓŠ²£Į§ČūµÄŹŌ¼ĮĘæŹ¢×°Na2SiO3ČÜŅŗ£¬Ń”ĻīA“ķĪó£»B”¢Ģ¼ĖįÄĘŹĒµē½āÖŹ£¬ČÜÓŚĖ®£¬Ģ¼ĖįÄĘÓ¦²šŠ“³ÉĄė×Ó£¬CO32££«2H£«=CO2”ü£«H2O£¬Ń”ĻīB“ķĪó£»C”¢ŹµŃéµÄÄæµÄŹĒŃéÖ¤ŃĪĖį”¢Ģ¼Ėį”¢¹čĖįĖįŠŌĒæČõ£¬¢ŁÖŠ·¢ÉśµÄ·“Ó¦£ŗCO32££«2H£«=CO2”ü£«H2O£¬ŃĪĖįĒæÓŚĢ¼Ėį£¬¢Ś·“Ó¦£ŗCO2£«H2O£«SiO32£=CO32££«H2SiO3£¬ĖµĆ÷Ģ¼ĖįµÄĖįŠŌĒæÓŚ¹čĖį£¬µ«ŹĒŃĪĖį¾ßÓŠ»Ó·¢ŠŌ£¬¢ŚÖŠŅ²ÓŠæÉÄÜŹĒ»Ó·¢³öµÄĀČ»ÆĒā²Ī¼Ó·“Ó¦£¬²śÉśøÉČÅ£¬Ń”ĻīC“ķĪó£»D”¢ĮņĖįŹĒÄѻӷ¢ŠŌĖį£¬¶ŌŗóĆꏵŃé²»²śÉśøÉČÅ£¬ÄÜĖµĆ÷ĖįŠŌ£ŗĮņĖį>Ģ¼Ėį>¹čĖį£¬Ń”ĻīDÕżČ·”£“š°øŃ”D”£


 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø 53ĢģĢģĮ·ĻµĮŠ“š°ø
53ĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°ŃNaHCO3ŗĶNa2CO3”¤10H2O»ģŗĶĪļ6.56gČÜÓŚĖ®ÖĘ³É100mLČÜŅŗ£¬²āµĆČÜŅŗÖŠc£ØNa£«£©=0.5mol/L”£ĻņøĆČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæŃĪĖįĒ”ŗĆĶźČ«·“Ó¦£¬½«ČÜŅŗÕōøÉŗó£¬ĖłµĆ¹ĢĢåÖŹĮæĪŖ
A. 2.93 g B. 5.85 g C. 6.56g D. ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ¼×”¢ŅŅ”¢±ū”¢XŹĒĖÄÖÖ֊ѧ»Æѧ֊³£¼ūµÄĪļÖŹ£¬Ęä×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®Ōņ¼×ŗĶX²»æÉÄÜŹĒ£Ø £©
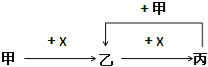
A. ¼×ĪŖC£¬XĪŖO2 B. ¼×ĪŖSO2£¬XĪŖNaOHČÜŅŗ
C. ¼×ĪŖFe£¬XĪŖCl2 D. ¼×ĪŖAlCl3£¬XĪŖNaOHČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧæĘŃŠŠ”×éŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäijŅ»Ģõ¼ž¶Ō»ÆŃ§Ę½ŗāµÄÓ°Ļģ£¬µĆµ½ČēĶ¼ĖłŹ¾±ä»Æ¹ęĀÉ£Øp±ķŹ¾Ń¹Ē棬T±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£ŗ 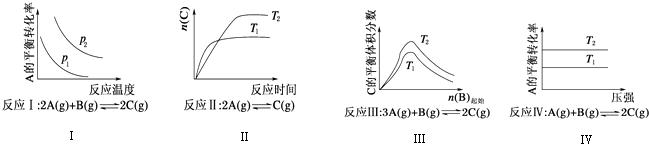
øł¾ŻŅŌÉĻ¹ęĀÉÅŠ¶Ļ£¬ĻĀĮŠ½įĀŪÕżČ·µÄŹĒ£Ø £©
A.·“Ó¦¢ń£ŗ”÷H£¾0£¬p2£¾p1
B.·“Ó¦¢ó£ŗ”÷H£¾0£¬T2£¾T1»ņ”÷H£¼0£¬T2£¼T1
C.·“Ó¦¢ņ£ŗ”÷H£¾0£¬T1£¾T2
D.·“Ó¦¢ō£ŗ”÷H£¼0£¬T2£¾T1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ£Ø £©
A. ĀĮ·ŪĶ¶Čėµ½NaOHČÜŅŗÖŠ£ŗ2Al+2OH£ØT2AlO2£+H2”ü
B. Ģś·ŪÓėĀČ»ÆĢśČÜŅŗ·“Ó¦£ŗ![]()
C. ĀČĘųÓėĖ®µÄ·“Ó¦£ŗCl2+ H2O ØT 2H+ + Cl- + ClO-
D. ĘÆ°×·ŪČÜŅŗÖŠĶØČė¹żĮæµÄCO2£ŗClO- + CO2 + H2O ØT HClO + HCO3£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ż³Ģ»ņĻÖĻóÓėŃĪĄąĖ®½āĪŽ¹ŲµÄŹĒ£Ø””””£©
A.“æ¼īČÜŅŗČ„ÓĶĪŪ
B.ĢśŌŚ³±ŹŖµÄ»·¾³ĻĀÉśŠā
C.¼ÓČČĀČ»ÆĢśČÜŅŗŃÕÉ«±äÉī
D.ÅØĮņ»ÆÄĘČÜŅŗÓŠ³ōĪ¶
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆČŪČŚ¼ī±ŗÉÕ¹¤ŅÕæÉ“ÓĀĮČČ·ØÉś²ś½šŹōøõµÄøõŌü£ØAl”¢Al2O3”¢Cr2O3µČ£©ÖŠ½ž³öøõŗĶĀĮ£¬ĪŖŹµĻÖøõŗĶĀĮµÄŌŁÉśĄūÓĆ”£Ę乤×÷Į÷³ĢČēĻĀ£ŗ
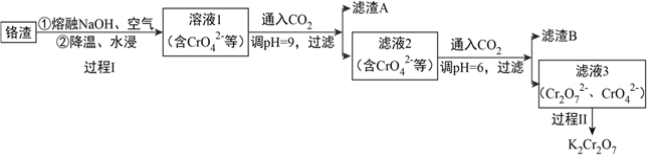
£Ø1£©ĀĮČČ·ØŅ±Į¶½šŹōøõ£¬ŹĒĄūÓĆĮĖ½šŹōĀĮµÄ__________£ØĢī”°Ńõ»ÆŠŌ”±»ņ”°»¹ŌŠŌ”±£©”£
£Ø2£©ČÜŅŗ1ÖŠµÄŅõĄė×ÓÓŠCrO42-”¢______”¢_______”£
£Ø3£©¹ż³ĢI£¬ŌŚCr2O3²ĪÓėµÄ·“Ó¦ÖŠ£¬ČōÉś³É0.4molCrO42-£¬ĻūŗÄŃõ»Æ¼ĮµÄĪļÖŹµÄĮæŹĒ__________”£
£Ø4£©ĶØČėCO2µ÷½ŚČÜŅŗpHŹµĻÖĪļÖŹµÄ·ÖĄė”£
¢ŁĀĖŌüAģŃÉÕµĆµ½Al2O3£¬ŌŁÓƵē½ā·ØŅ±Į¶Al”£Ņ±Į¶AlµÄ»Æѧ·½³ĢŹ½ŹĒ____________________”£
¢ŚĀĖŌüBŹÜČČ·Ö½āĖłµĆĪļÖŹµÄ²ĪÓėŃ»·ĄūÓĆ£¬BŹĒ__________”£
¢ŪŅŃÖŖ£ŗ2CrO42-+2H+ ![]() Cr2O72-+H2O K=4.0”Į1014
Cr2O72-+H2O K=4.0”Į1014
ĀĖŅŗ3ÖŠCr2O72-µÄÅØ¶ČŹĒ0.04mol/L£¬ŌņCrO42-µÄÅØ¶ČŹĒ__________mol/L”£
£Ø5£©¹ż³ĢIIµÄÄæµÄŹĒµĆµ½K2Cr2O7“ÖĘ·”£
²»Ķ¬ĪĀ¶ČĻĀ»ÆŗĻĪļµÄČܽā¶Č£Øg/100gH2O£©
»ÆŗĻĪļĆū³Ę | 0”ę | 20”ę | 40”ę | 60”ę | 80”ę |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
½įŗĻ±ķÖŠŹż¾Ż·ÖĪö£¬¹ż³ĢIIµÄ²Ł×÷ŹĒ£ŗ__________________________£¬¹żĀĖ£¬µĆµ½K2Cr2O7“ÖĘ·”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
A.½« AgCl ·ÅČėĖ®ÖŠ²»Äܵ¼µē£¬¹Ź AgCl ²»ŹĒµē½āÖŹ
B.CO2ČÜÓŚĖ®µĆµ½µÄČÜŅŗÄܵ¼µē£¬µ« CO2ŹōÓŚ·Ēµē½āÖŹ
C.½šŹōÄܵ¼µē£¬ĖłŅŌ½šŹōŹĒµē½āÖŹ
D.ŅŗĢ¬ HCl ²»µ¼µē£¬ HCl ŹōÓŚ·Ēµē½āÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄ½į¹¹”¢ŠŌÖŹµČŠÅĻ¢ČēĻĀ±ķĖłŹö£ŗ
ŌŖĖŲ | ½į¹¹”¢ŠŌÖŹµČŠÅĻ¢ |
A | ŹĒ¶ĢÖÜĘŚÖŠ£Ø³żĻ”ÓŠĘųĢåĶā£©Ō×Ó°ė¾¶×ī“óµÄŌŖĖŲ£¬øĆŌŖĖŲµÄijÖÖŗĻ½šŹĒŌ×Ó·“Ó¦¶ŃµÄµ¼ČČ¼Į |
B | BÓėAĶ¬ÖÜĘŚ£¬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ³ŹĮ½ŠŌ |
C | ŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļ¼«Ņ×ČÜÓŚĖ®£¬æÉÓĆ×÷ÖĘĄä¼Į |
D | ŹĒŗ£Ė®ÖŠ³żĒā”¢ŃõŌŖĖŲĶāŗ¬Įæ×ī¶ąµÄŌŖĖŲ£¬Ę䵄֏»ņ»ÆŗĻĪļŅ²ŹĒ×ŌĄ“Ė®Éś²ś¹ż³ĢÖŠ³£ÓƵÄĻū¶¾É±¾ś¼Į |
Ēėøł¾Ż±ķÖŠŠÅĻ¢ĢīŠ“£ŗ
£Ø1£©AŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ £®
£Ø2£©BŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ£»Ąė×Ó°ė¾¶£ŗBA£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©£®
£Ø3£©CŌ×ӵĵē×ÓÅŲ¼Ķ¼ŹĒ £¬ ĘäŌ×ÓŗĖĶāÓŠøöĪ“³É¶Ōµē×Ó£¬ÄÜĮæ×īøߵĵē×ÓĪŖ¹ģµĄÉĻµÄµē×Ó£¬Ęä¹ģµĄ³ŹŠĪ£®
£Ø4£©DŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ £¬ D©µÄ½į¹¹Ź¾ŅāĶ¼ŹĒ £®
£Ø5£©BµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÓėAµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖÓėDµÄĒā»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com