
【题目】在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CON2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( ) 
A.加催化剂
B.降低温度
C.增大NO的浓度
D.缩小容器体积
【答案】B
【解析】解:A.催化剂对平衡移动无影响,转化率不变,故A不选; B.降低温度,反应速率减小,平衡正向移动,转化率增大,与图象一致,故B选;
C.增大NO的浓度,反应速率增大,NO的转化率减小,故C不选;
D.缩小体积,压强增大,反应速率加快,故D不选;
故选B.
【考点精析】通过灵活运用化学平衡状态本质及特征,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


科目:高中化学 来源: 题型:
【题目】T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
(1)写出该反应的化学方程式 .
(2)反应开始至3min时,用D表示的平均反应速率为mol/(Lmin).
(3)T℃时,该反应的化学平衡常数K= .
(4)第6min时,保持温度不变,将容器的体积缩小至原来的一半,重新达到平衡后,D的体积分数为 .
物质 | A | B | D | E |
物质的量mol | 0.8 | 1.0 | 0.4 | 0.2 |
(5)另有一个2L的密闭容器,T℃、某一时刻时,容器中各物质的量如表所示:此时v(正)v(逆)(填“大于”或“等于”或“小于”). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( ) 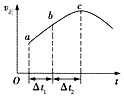
A.反应物的总能量低于生成物的总能量
B.△t1=△t2时,CO的转化率:a~b段小于bc段
C.反应在c点达到平衡状态
D.反应物浓度:a点小于b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下几个热化学方程式,能表示有关物质燃烧时的燃烧热的热化学方程式是( )
A.C(s)+ ![]() O2(g)═CO(g)△H=+110.5 kJ?mol﹣1
O2(g)═CO(g)△H=+110.5 kJ?mol﹣1
B.C(s)+O2(g)═CO2(g)△H=﹣393.5 kJ?mol﹣1
C.2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ?mol﹣1
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8 kJ?mol﹣1
O2(g)═H2O(g)△H=﹣241.8 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取25.0gCuSO45H2O晶体,加热使之均匀、缓慢升温至1000℃并恒温1小时,试通过计算回答下列问题(如果是混合物,要算出混合物中各组分的质量):
(1)在某中间温度时,固体产物质量是否可能为10g?
(2)不考虑实验带来的误差,在反应条件下,反应气态产物除去水后,物质的量可能为
A.0mol
B.0.1mol
C.大于0.1mol
(3)你认为最终固体产物为多少克?产物颜色如何?
(4)如果某同学做此实验时最后固体质量为7.6g,试计算其组分.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与1 mol·L-1 H2SO4反应制取氢气时,下列措施不能使氢气生成速率加快的是
A. 加入少量的CuSO4溶液B. 改用18 mol·L-1硫酸溶液反应
C. 不用铁片,改用铁粉D. 加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是
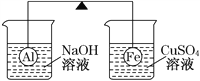
A. 铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边下沉
B. 铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
C. 反应后去掉两烧杯,杠杆仍平衡
D. 右边球上出现红色,左边溶液的c(OH-)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石英(SiO2)系列光纤,具有低耗、宽带的特点,已广泛应用于有线电视和通信系统。SiO2属于( )
A. 氧化物 B. 酸 C. 碱 D. 盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com