
���� ���ᡢ��������Һ��̼������Һ������ͭ��Һ������������Һ������Һ�У�����ͭ��Һ����ɫ��Һ������ֱ��ͨ���۲쿴��������A��Ҫ��ʵ��ֱ��ȷ������֪A��������ͭ��Һ������ͭ��Һ���������ֻ�ϣ�ֻ��������ʱ���κ�����BΪ���ᣬ��ʣ���������Һ��μ����ᣬ��������Һ�����ְ�ɫ������̼������Һ��������ݲ�����ֻ������������Һ�����������ݴ˷������⣻
��� �⣺���ᡢ��������Һ��̼������Һ������ͭ��Һ������������Һ������Һ�У�����ͭ��Һ����ɫ��Һ������ֱ��ͨ���۲쿴��������A��Ҫ��ʵ��ֱ��ȷ������֪A��������ͭ��Һ������ͭ��Һ���������ֻ�ϣ�ֻ��������ʱ���κ�����BΪ���ᣬ��ʣ���������Һ��μ����ᣬ��������Һ�����ְ�ɫ������̼������Һ��������ݲ�����ֻ������������Һ��������������CΪ̼���ƣ�DΪ����������
��1�����ݷ�����֪AΪ����ͭ��Һ��C��̼������Һ���ʴ�Ϊ��CuSO4��Na2CO3��
��2��̼������Һ��μ��������ɶ�����̼��������Ӧ�����ӷ�Ӧ����ʽΪCO32-+2H+=H2O+CO2��������ͭ��Һ������������Ͽɵõ����ᱵ��������ͭ������������Ӧ�����ӷ�Ӧ����ʽΪBa2++2OH-+SO42-+Cu2+=Cu��OH��2��+BaSO4�������������������Һ��Ӧ�����ӷ���ʽΪOH-+H+=H2O���ʴ�Ϊ��CO32-+2H+=H2O+CO2����Ba2++2OH-+SO42-+Cu2+=Cu��OH��2��+BaSO4����OH-+H+=H2O��
���� ���������ʵļ��������壬�������ӷ�Ӧ�����ӷ�Ӧ����ʽ����д���������Կ��飬�ѶȲ���������˫����ϰ����ʵ��������߷������⡢��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ�������Һ�ĵ���������һ�������������Һ�ĵ�������ǿ | |
| B�� | Ӱ�컯ѧƽ�ⳣ�����������¶� | |
| C�� | ���ȷ�Ӧ��һ�����Է����У������ȷ�ӦҲ�����Է����� | |
| D�� | ������ķ�Ӧ���ʱ�һ�������ʱ�����ķ�Ӧ���ز�һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
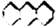 ������ȴ����ͬ���칹�干�У������������칹����������
������ȴ����ͬ���칹�干�У������������칹����������| A�� | 14�� | B�� | 15�� | C�� | 16�� | D�� | 17�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ�м��˹�����ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| B�� | ����ʯ��ˮ�����С�մ���Һ��ϣ�Ca2++OH-+HCO3-�TCaCO3��+H2O | |
| C�� | ��1molFeBr2��Һ��ͨ�� 1.5molCl2 ��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl- | |
| D�� | �Ȼ�������Һ��ͨ��������Fe2++Cl2�TFe3++2C1- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�8 g O2����5NA������ | |
| B�� | 1 L 1.0 mol•L-1NaAlO2��Һ�к�����ԭ����Ϊ2NA | |
| C�� | ��״���£�2.24 L CCl4�к��еķ�����Ϊ0.1NA | |
| D�� | ����ͭ�Ĺ����У�����������32 gͭʱת�Ƶĵ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | x=0.5y | B�� | x=0.1+0.5y | C�� | y=2��x-0.1�� | D�� | y=2x-0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaAlO2��Һ | B�� | Na2SiO3��Һ | C�� | ��������Һ | D�� | CaCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijС����CoCl2•6H2O��NH4Cl��H2O2��Ũ��ˮΪԭ�ϣ��ڻ���̿���£��ϳɳȻ�ɫ����X��Ϊȷ������ɣ���������ʵ�飮
ijС����CoCl2•6H2O��NH4Cl��H2O2��Ũ��ˮΪԭ�ϣ��ڻ���̿���£��ϳɳȻ�ɫ����X��Ϊȷ������ɣ���������ʵ�飮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com