
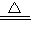 MnCl2+Cl2↑+2H2O,根据二氧化锰和盐酸的物质的量判断反应的过量问题,结合方程式计算相关物理量.
MnCl2+Cl2↑+2H2O,根据二氧化锰和盐酸的物质的量判断反应的过量问题,结合方程式计算相关物理量.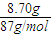 =0.10mol.n(HCl)=
=0.10mol.n(HCl)= =1.2mol,
=1.2mol, MnCl2+Cl2↑+2H2O可知二氧化锰不足,完全反应,则
MnCl2+Cl2↑+2H2O可知二氧化锰不足,完全反应,则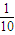 ×1.0mol=0.10mol;
×1.0mol=0.10mol;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分).8.70g MnO2与100mL 37.0%密度为1.19g/cm3的浓盐酸共热(假设HCI没有损失),反应结束后,将剩余的溶液加水稀释至100mL。取出10mL溶液加入足量AgNO3溶液,有白色沉淀生成。求:
(1)反应中生成的Cl2在标准状况下的体积.
(2)10.0mL溶液加入AgNO3溶液后生成沉淀的质量.
查看答案和解析>>
科目:高中化学 来源:2011年山东省潍坊市新高二化学暑假作业(一) 题型:计算题
(8分).8.70g MnO2与100mL 37.0%密度为1.19g/cm3的浓盐酸共热(假设HCI没有损失),反应结束后,将剩余的溶液加水稀释至100mL。取出10mL溶液加入足量AgNO3溶液,有白色沉淀生成。求:
(1)反应中生成的Cl2在标准状况下的体积.
(2)10.0mL溶液加入AgNO3溶液后生成沉淀的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:
.8.70g MnO2与100mL 37.0%密度为1.19g/cm3的浓盐酸共热(假设HCI没有损失),反应结束后,将剩余的溶液加水稀释至100mL。取出10mL溶液加入足量AgNO3溶液,有白色沉淀生成。求(1)反应中生成的Cl2在标准状况下的体积.
(2)10.0mL溶液加入AgNO3溶液后生成沉淀的质量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com