
人体正常的血红蛋白中应含Fe2+,若误食亚硝酸盐,则导致血红蛋白中Fe2+转化为高铁血红蛋白而中毒,服用维生素C可解除亚硝酸盐中毒.下列叙述中正确的是( )
|
| A. | 亚硝酸盐是还原剂 | B. | 维生素C被还原 |
|
| C. | 维生素C将Fe2+氧化为Fe3+ | D. | 亚硝酸盐是氧化剂 |
考点:
氧化还原反应.
专题:
氧化还原反应专题.
分析:
由亚硝酸钠导致血红蛋白中的Fe2+转化为高铁血红蛋白而中毒,服用维生素C可解除亚硝酸钠中毒,则服用维生素C中某元素的化合价升高,以此来解答.
解答:
解:A.亚硝酸钠导致血红蛋白中的Fe2+转化为高铁血红蛋白而中毒,Fe元素的化合价升高,则亚硝酸钠表现了氧化性,故A错误;
B.服用维生素C可解除亚硝酸钠中毒,则服用维生素C中某元素的化合价升高,所以维生素C作还原剂,被氧化,故B正确错误;
C.维生素C将Fe3+还原成Fe2+,故C错误;
D.亚硝酸钠将Fe2+转化为高铁血红蛋白,是氧化剂,故D正确
故选D.
点评:
本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注重利用信息与氧化还原反应中的概念来解答,题目难度不大.


科目:高中化学 来源: 题型:
为预防“H1N1”甲型流感,同学们每天用“84”消毒液(NaClO溶液)消毒,下列说法不正确的是()
A. NaClO溶液的消毒原理是使蛋白质变性
B. 1 mol Cl2与足量NaOH溶液反应转移2 mol电子
C. NaClO溶液的漂白原理与Na2O2相同,与SO2不同
D. “84”消毒液与“洁厕灵”(盐酸)混合使用可能会产生有毒的氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.则下列分析与判断不正确的是(不计CO2溶解)()
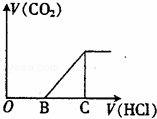
A. 若OB=0,则形成溶液M所发生反应的离子方程式为OH﹣+CO2═HCO3﹣
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32﹣和HCO3﹣
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
用饱和的FeCl3溶液制取Fe(OH)3胶体,正确的操作是( )
|
| A. | 将FeCl3溶液滴人蒸馏水中 |
|
| B. | 将FeCl3溶液滴人热水中,生成棕黄色液体 |
|
| C. | 将FeCl3溶液滴人沸水中,并继续煮沸至生成红褐色液体 |
|
| D. | 将FeCl3溶液滴人沸水中,并继续煮沸至生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在 Mg+H2SO4=MgSO4+H2↑中,氧化剂与还原剂的物质的量之比为 ;
(2)在3Cl2+6KOH=5KCl+KClO3+3H2O 中,氧化剂与还原剂质量之比为 ;
(3)在2H2S+SO2=3S↓+2H2O 中,氧化产物与还原产物的质量之比为 ;
(4)MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O中被氧化和未被氧化的Cl﹣的个数比为 ;
(5)在 3NO2+H2O=2HNO3+NO 中,每生成2mol NO,转移的电子数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
除去某物质里混有的少量杂质,下列做法中不正确的是(括号内的物质为杂质)()
A. KNO3溶液(AgNO3):加足量KCl溶液后过滤.
B. NaCl溶液(Na2CO3):加足量盐酸后加热.
C. KNO3固体(NaCl):溶解后加热蒸发得浓溶液,降温结晶后过滤.
D. NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是()
A. 常温下,淀粉遇I﹣ 变蓝色
B. 油脂水解可得到氨基酸和甘油
C. 所有烷烃和蛋白质中都只存在碳碳单键
D. 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去).图中K为止水夹(处于关闭状态),F是一半空的注射器.
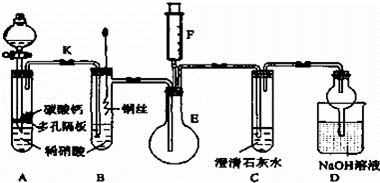
请回答有关问题:
(1)设计装置A的目的是利 为达到此目的,应进行的操作是 .
(2)在完成(1)中的操作后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是 .B中反应的离子方程式为: .
(3)装置E和F的作用是 .为实现此作用,其操作方法是 .
(4)装置D的作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com