
【题目】五种短周期元素A、B、C、D、E的性质及结构信息如下:
① 原子半径A>B>C>D>E;
② 五种元素之间形成的常见的四种分子如下:
甲 | 乙 | 丙 | 丁 | |
比例模型 |
|
|
|
|
组成元素 | D、E | B、E | A、D、E | C、E |
电子总数 | 10 | 18 | 26 | 10 |
请根据上述信息回答下列问题:
(1)A元素的单质与物质甲发生反应的离子方程式为__________,其化学反应平衡常数的表达式为_______。
(2)戊与乙互为同系物,有五种同分异构体,戊的分子式为_____,己与乙具有相同的电子数,与甲含有的元素种类相同,己分子的结构式为_______。
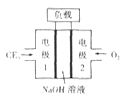
(3)C与E元素组成的CE3与液氮可组成燃料电池,产物均为无污染的物质,可用于驱动潜艇,燃料电池装置如下图所示。该电池的负极反应式为_____。电池工作时OH-向_____移动(填“正极”或“负极”)。
(4)B与D组成的一种物质在自然界中可循环,循环时其与CaCO3反应。已知Ksp(CaCO3)=2.8×10-9,现将CaCl2溶液与Na2CO3溶液等体积混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀的最小浓度为__________(忽略混合前后溶液的体积变化)。
【答案】 Cl2+H2O=Cl-+H++HClO 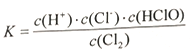 C6H14 H-O-O-H 2NH3-6e-+6OH-=N2+6H2O 负极 5.6×10-5mol/L
C6H14 H-O-O-H 2NH3-6e-+6OH-=N2+6H2O 负极 5.6×10-5mol/L
【解析】根据五种元素之间形成的常见的四种分子的比例模型结合原子半径A>B>C>D>E,可知,甲为水分子,乙为乙烷分子,丙为HClO分子,丁为氨气分子,则A为Cl、B为C、C为N、D为O、E为H。
(1)氯气与水反应的离子方程式为Cl2+H2O=Cl-+H++HClO,其化学反应平衡常数的表达式K=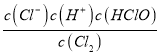 ,故答案为:Cl2+H2O=Cl-+H++HClO;K=
,故答案为:Cl2+H2O=Cl-+H++HClO;K=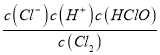 ;
;
(2)有五种同分异构体的烷烃的分子式为C6H14,己与乙烷具有相同的电子数,与水含有的元素种类相同,则己为过氧化氢,结构式为H-O-O-H,故答案为:C6H14; H-O-O-H;
(3)NH3与液氮可组成燃料电池,产物均为无污染的物质,水和氮气,氨气在负极发生氧化反应,电极反应式为2NH3-6e-+6OH-=N2+6H2O,根据电极反应式,电池工作时OH-向负极移动,故答案为:2NH3-6e-+6OH-=N2+6H2O;负极;
(4) Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=1×10-4mol/L,根据Ksp=c(CO32-)c(Ca2+)=2.8×10-9可知,c(Ca2+)=![]() mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L,故答案为:5.6×10-5mol/L。
mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L,故答案为:5.6×10-5mol/L。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.乙烯水化制乙醇;溴乙烷水解制乙醇
B.由乙醇制乙烯;溴乙烷与氢氧化钠醇溶液共热制乙烯
C.苯硝化制硝基苯;乙烯使酸性高锰酸钾溶液褪色
D.甲苯使酸性高锰酸钾溶液褪色;丙炔使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物的物质的量一定时,组内各物质按任意比混合,完全燃烧时耗O2的量不变的是
A. 甲烷、甲醇、甲醛 B. 丙烯酸(CH2=CH-COOH)、乙烯、乙醇
C. 丙烯、2-丁烯、环已烷 D. 乙炔、苯、1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知-C6H5 代表苯基,下列卤代烃在 KOH 醇溶液中加热能发生消去反应的有( )种
① C6H5Br ②CH3Cl ③(CH3)3CCH2Cl ④C6H5CH2Br ⑤ CHCl2-CHBr2 ⑥(CH3)3CCl
A.1B.2C.3D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 生石灰能与水反应,可用于实验室干燥氯气
B. NO2、、SO2二种气体都能与水反应生成酸,它们都是酸性氧化物
C. SO2、NOx的大量排放会导致酸雨的发生
D. 高温下,二氧化硅与碳酸钠反应放出CO2,可说明硅酸的酸性比碳酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯净物X、Y、Z转化关系如图所示,下列判断正确的是( )

A. X可能是金属铜 B. Y不可能是氢气
C. Z可能是氯化钠 D. Z可能是三氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室安卡因(G)是一种抗心律失常药物,可由下列路线合成:
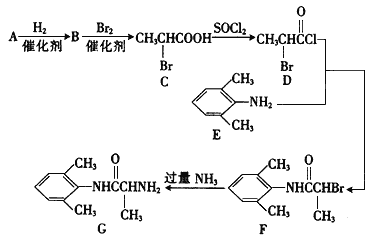
I.(1)己知A是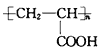 的单体,则A中所含官能团的名称是____________。
的单体,则A中所含官能团的名称是____________。
(2)写出B的结构简式并用系统命名法给C命名: B:_____________, C的名称:____________。
(3)L是E的同分异构体,L分子中含有苯环,且苯环上一氯代物只有两种,则L所有可能的结构简式有![]() 、__________________。
、__________________。
(4)F →G的反应类型是_______________。
(5)下列关于室安卡因(G)的说法正确的是____________。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d.属于氨基酸
(6)写出C与足量NaOH醇溶液共热时反应的化学方程式:______________。
II. H是C的同系物,其核磁共振氢谱有两个峰。按如下路线,由H可合成高聚物V:
![]()
(7)H的结构简式为_________________;N→Q的反应类型为________________。
(8)写出Q→V的反应方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有A、B、C、D、E、F六种装置,如图所示。(胶塞、导管可自由选用)


(1)写出①~④的仪器名称:①__________,②__________,③________,④________。
(2)实验室制取并收集氧气时应选择________和________相连接,制取并收集氢气时应选择________和________相连接。
(3)做木炭还原氧化铜并检验生成气体的实验,应选择________和________相连接,检验气体时观察到的实验现象是__________________________________________________。
(4)制取氢气并做还原氧化铜的实验,应选择________和________装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,其原因是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com