
【题目】短周期元素X、Y、Z原子序数之和为16,原子半径大小为r(Y)>r(X)>r(Z),它们的常见单质在适当条件下可发生如图变化,其中B和C均为10电子分子。下列说法不正确的是( )

A.X与Z形成的某种化合物可用来杀菌消毒
B.自然界中X单质与Y单质不能发生化学反应
C.B和C分子间因形成氢键而使C极易溶于B中
D.A和C一定条件下能发生氧化还原反应
【答案】B
【解析】
常见的10电子分子有CH4、NH3、H2O、HF,则Z单质一定为H2,Z为H;X、Y、Z原子序数之和为16,则X、Y原子序数只和=16-1=15,原子半径大小为r(Y)>r(X)>r(Z),X、Y分别为O、N或F、C,且X单质能和Y单质反应,则X、Y确定为O、N;综上所述,X、Y、Z分别为:O、N、H,A为NO,B为H2O,C为NH3,据此解答。
A.X(O)与Z(H)形成的H2O2有强氧化性,能使细菌的蛋白质变性,可用来杀菌消毒,A正确;
B.自然界中的X单质(O2)与Y单质(N2)在放电的条件下能反应生成NO,B错误;
C.B为H2O,C为NH3,H2O和NH3分子间容易形成氢键而使NH3极易溶于H2O中,C正确;
D.A为NO,有一定氧化性,C为NH3,有较强还原性,一定条件下能发生氧化还原反应,D正确。
答案选B。


科目:高中化学 来源: 题型:
【题目】将一定量A、B装入容积为1 L的恒温密闭容器中,发生反应:2A(g)+mB(g)![]() nC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8x mol·L-1。下列说法正确的是( )
nC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8x mol·L-1。下列说法正确的是( )
A.化学计量数的关系为2+m <n
B.容器的容积缩小,正反应速率增大,逆反应速率减小
C.原容器中用B表示的该反应在1min内的平均速率为![]() mol·(L·min)-1
mol·(L·min)-1
D.若保持温度和容器容积不变,充入氦气,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解,100℃左右时升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不相同,分别如(I)和(Ⅱ)所示,
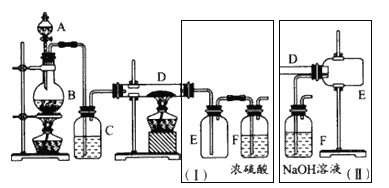
试回答:
(1)B中反应的化学方程式为___________________________。
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是______________。
(3)D中反应的化学方程式为______________________________。
(4)装置(I)的主要缺点是_______________________。
(5)装置(Ⅱ)的主要缺点是______________________________,如果选用此装置来完成实验,则必须采取的改进措施是:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“新冠病毒”疫情让人们再次认识到化学的重要性。下列有关抗疫物资的化学用语表示正确的是( )
A.中子数为127的碘原子:![]()
B.供氧剂中过氧化钙(CaO2)的电子式:![]()
C.84消毒液中次氯酸钠的电离方程式:NaClO![]() Na++ClO-
Na++ClO-
D.口罩“熔喷层”原料中聚丙烯的结构简式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是

A. 反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 图中X点所示条件下,延长反应时间能提高NO转化率
C. 图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁的一个反应如下: CO(g)+FeO(s)![]() CO2(g)+Fe(s),△H>0已知1100℃时K=0.263
CO2(g)+Fe(s),△H>0已知1100℃时K=0.263
(1)其平衡常数的表达式为K=___。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值___(填“增大”“减小”或“不变”下同),平衡常数K的变化是___。如果温度不变,在原平衡体系中继续加入一定量CO,达新平衡时,CO的体积分数和原平衡相比___。
(2)1100℃时,若测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应___(填“已经”或“没有”)处于化学平衡状态,此时化学反应速率是v(正)___(填“大于”“小于”或“等于”)v(逆)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为(CO,CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
ii:CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
iii:CH3OH(g)![]() CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
化学键 | H—H | C=O | C≡O | H—O |
E/KJ·mol-1 | 436 | 803 | 1076 | 465 |
由此计算ΔH2=___kJ·mol-1。已知ΔH1=-63kJ·mol-1,则ΔH3=___kJ·mol-1。
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:
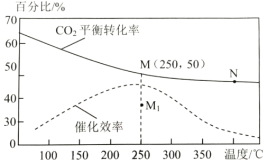
①下列说法不正确的是(__________)
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为___,250℃时反应的平衡常数Kp=___(MPa)-2(保留三位有效数字);
③若要进一步提高甲醇产率,可采取的措施有___(写两条即可)
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:___。
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)![]() CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
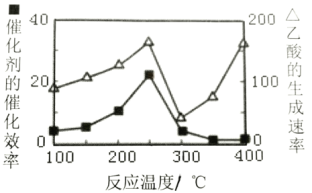
250~300℃时,乙酸的生成速率降低的主要原因是___。
300~400℃时,乙酸的生成速率升高的主要原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,x A + y B ![]() z C的反应达到平衡。
z C的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是_______。
(2)加热后C的质量分数减少,正反应是___________________反应。(填“吸热”或“放热”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白屈菜有止痛、止咳等功效,从其中提取的白屈菜酸的结构简式如图所示。下列有关白屈菜酸的说法中不正确的是( )

A.白屈菜酸的同分异构体中可能含有芳香族化合物
B.所有碳原子可以共面
C.1mol白屈菜酸完全燃烧需要O2的物质的量为4mol
D.能通过加聚反应形成高分子物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com