
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
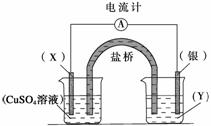
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的__________极,发生的电极反应为______________________;
X电极上发生的电极反应为______________________________________________;
(3)外电路中的电子是从__________电极流向__________电极。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列条件下的X溶液均能跟少量盐酸反应,其中反应速率最快的是
A.10℃ 20 mL 3mol/L的X溶液 B.20℃ 30 mL 2mol/L的X溶液
C.20℃ 10 mL 4mol/L的X溶液 D.10℃ 10 mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
1)金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型。
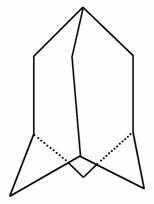
金刚烷
①金刚烷的分子式为________;
②根据中学学过的同分异构体判断规则,判断由溴原子取代分子中的氢原子形成的一溴代物有________种。
(2)“立方烷”是一种 新合成的烃,其分子为正方体结构,其碳架结构如图所示。
新合成的烃,其分子为正方体结构,其碳架结构如图所示。

①立方烷的分子式为________;
②该立方烷的二氯代物具有同分异构体的数目是______;
③该立方烷的六氯代物具有同分异构体的数目是______;
④将a g立方烷溶于b mL苯中,然后通入c L乙炔(标准状况下),所得混合物中碳的百分含量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
选择下列某种答案的序号, 填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
| 物质 名称 | 丁烷与 2--甲基丙烷 | 红磷 与白磷 | 庚烷与 十六烷 | 氯仿与 三氯甲烷 | 氕与 氘、氚 | 新戊烷与 2,2--二甲基丁烷 | 2--甲基戊烷与 2,3--二甲基丁烷 |
| 相互 关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各装置中都盛有0.1 mol·L-1的NaCl溶液,放置一定时间后,装置中的四块相同的锌片,腐蚀速率由快到慢的正确顺序是( )
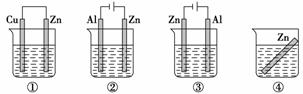
A.③①④② B.①②④③ C.①②③④ D.②①④③
查看答案和解析>>
科目:高中化学 来源: 题型:
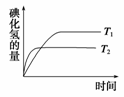
在密闭容器中进行如下反应:H2(g)+I2(g)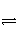
 2HI(g)。在温度T1和T2时,产物的量与反应时间的关系如图所示。符合如图所示的正确判断是( )
2HI(g)。在温度T1和T2时,产物的量与反应时间的关系如图所示。符合如图所示的正确判断是( )
A.T1>T2,ΔH>0 B.T1>T2,ΔH<0
C.T1<T2,ΔH>0 D.T1<T2,ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(1)根据表中数据,在该题图中相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
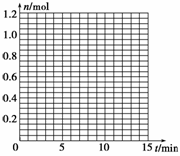
(2)体系中发生反应的化学方程式是____________;
(3)列式计算该反应在0~3 min时间内产物Z的平均反应速率:__________________;
(1) 该反应达到平衡时反应物X的转化率α等于___________________________;
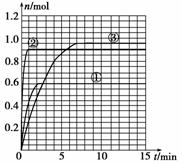
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如上图所示),则曲线①、②、③改变的实验条件分别是:
①________;②________;③________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NO和CO都是汽车尾气中的有害物质,它们能缓慢地反应生成氮气和二氧化碳,对此反应,下列叙述正确的是()
A. 使用适当的催化剂不改变反应速率
B. 降低压强能增大反应速率
C. 升高温度能增大反应速率
D. 改变压强对反应速率无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO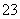 和OH-
和OH-
B.NaHCO3溶液中:[H+]+[H2CO3]=[OH-]
C.10 mL 0.10 mol·L-1 CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:[Na+]>[CH3COO-]>[OH-]>[H+]
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com