
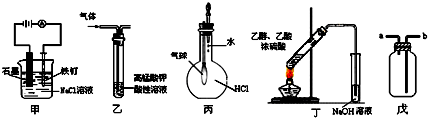
| A、①⑤ | B、④⑤ | C、①② | D、③⑤ |


科目:高中化学 来源: 题型:
| A、V(A)平:V(B)平=5:3 |
| B、A的转化率为20% |
| C、x:y=2:1 |
| D、D的反应速率为0.25 mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲和丁的最简式相同 |
| B、丁的分子量是丙的两倍 |
| C、甲既可是饱和一元醛,又可是饱和一元酮 |
| D、甲的分子中一定具有甲基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘水不可用于鉴别苯、四氯化碳、乙醇三种无色液体 |
| B、氢气还原氧化铜实验先加热再通氢气 |
| C、配制一定物质的量浓度的硫酸溶液时.只需使用1次玻璃棒 |
| D、欲从碘水中分离出I2,可将适量的CCl4加入碘水中振荡静置分层后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、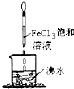 继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
B、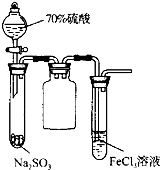 实验试管中出现淡黄色浑浊 |
C、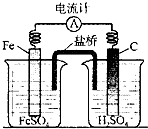 实验中碳棒上有无色气泡产生 |
D、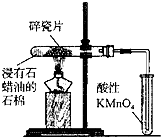 实验中酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:
A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:查看答案和解析>>
科目:高中化学 来源: 题型:
 已知X是一种盐,H是常见的金属单质,F、I是常见的非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.试回答下列问题:
已知X是一种盐,H是常见的金属单质,F、I是常见的非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com