
A.0.1 mol·L-1 B.0.2 mol·L-1?
C.0.3 mol·L-1 D.0.4 mol·L-1
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
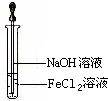 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:021
在氯化铝和硫酸铝的混合溶液中,当Al3+和![]()
![]() 的物质的量浓度相同时,则下列有关判断正确的是 ( )
的物质的量浓度相同时,则下列有关判断正确的是 ( )
A.3c(Al3+)=c(Cl-)
B.c(![]()
![]() )= c(Cl-)
)= c(Cl-)
C.c(![]()
![]() )< c(Cl-)
D.
)< c(Cl-)
D.![]() =
=![]()
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:021
A.3 c(Al3+)= c(Cl-)
B.c(SO![]() )= c(Cl-)
)= c(Cl-)
C.c(SO![]() )< c(Cl-)
D.c(Al2(SO4)3)=c(AlCl3)
)< c(Cl-)
D.c(Al2(SO4)3)=c(AlCl3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com