
【题目】若用AG表示溶液的酸度,其表达式为:AG=lg[ ]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是( )
]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10mL0.10mol/LMOH溶液,滴定曲线如图所示,下列说法正确的是( )

A. MOH电离方程式是MOH=M++OH-
B. C点加入盐酸的体积为10mL
C. 若B点加入的盐酸溶液体积为5mL,所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH-)
D. 滴定过程中从A点到D点溶液中水的电离程度逐渐增大
【答案】C
【解析】
A、没有滴入盐酸时,MOH的AG=-8,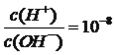 ,根据水的离子积Kw=c(H+)×c(OH-)=10-14,解出c(OH-)=10-3mol·L-1,因此MOH为弱碱,电离方程式为MOH=M++OH-,故A错误;B、C点时AG=0,即c(H+)=c(OH-),溶液显中性,MOH为弱碱,溶液显中性时,此时溶质为MOH和MCl,因此消耗HCl的体积小于10mL,故B错误;C、B点加入盐酸溶液的体积为5mL,此时溶液中溶质为MOH和MCl,且两者物质的量相等,根据电荷守恒,由c(M+)+c(H+)=c(Cl-)+c(OH-),根据物料守恒,c(M+)+c(MOH)=2c(Cl-),两式合并得到c(M+)+2c(H+)=c(MOH) + 2c(OH-),故C正确;D、随着HCl的滴加,当滴加盐酸的体积为10mL时,水电离程度逐渐增大,当盐酸过量,对水的电离程度起到抑制,故D错误。
,根据水的离子积Kw=c(H+)×c(OH-)=10-14,解出c(OH-)=10-3mol·L-1,因此MOH为弱碱,电离方程式为MOH=M++OH-,故A错误;B、C点时AG=0,即c(H+)=c(OH-),溶液显中性,MOH为弱碱,溶液显中性时,此时溶质为MOH和MCl,因此消耗HCl的体积小于10mL,故B错误;C、B点加入盐酸溶液的体积为5mL,此时溶液中溶质为MOH和MCl,且两者物质的量相等,根据电荷守恒,由c(M+)+c(H+)=c(Cl-)+c(OH-),根据物料守恒,c(M+)+c(MOH)=2c(Cl-),两式合并得到c(M+)+2c(H+)=c(MOH) + 2c(OH-),故C正确;D、随着HCl的滴加,当滴加盐酸的体积为10mL时,水电离程度逐渐增大,当盐酸过量,对水的电离程度起到抑制,故D错误。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿( PbS)直接制备硫酸铅粉末的流程如下:
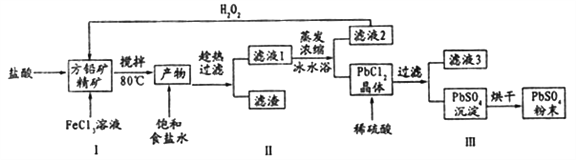
已知:(i) PbCl2 (s)+2C1-(aq)=PbCl42-(aq) △H>0
(ii)有关物质的Ksp和沉淀时的pH如下:
物质 | Ksp | 物质 | 开始沉淀时pH | 完全沉淀时pH |
PbSO4 | 1.0×10-8 | Fe(OH)3 | 2.7 | 3.7 |
PbCl2 | 1.6×10-5 | Pb(OH)2 | 6 | 7.04 |
(1)步骤I反应加入盐酸后可以观察到淡黄色沉淀生成,请写出的离子方程式___________。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因____________。
(3)在上述生产过程中可以循环利用的物质有______________。
(4)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式________________。
(5)铅的冶炼、加工会使水体中重金属铅的含量增大造成严重污染。某课题组制备了一种新型脱铅剂(用EH表示),能有效去除水中的痕量铅,脱铅过程中主要发生的反应为:2EH(s)+Pb2+![]() E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
A.4~5 B.6~7 C.9~10 D.11~12
(6)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KC1混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Li+向_______移动(填“负极”或“正极”)。
②负极反应式为_____________。
③电路中每转移0.2mol电子,理论上生成_________g Pb。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)羟基的电子式________________;
(2)电石气的分子式___________;
(3)顺式-2-丁烯的结构简式__________________;
(4)![]() 的系统命名___________________________;
的系统命名___________________________;
(5)写出由甲苯制TNT的方程式_________________________________________
(6)2﹣甲基﹣1、3﹣丁二烯与等物质的量的Br2发生加成反应,产物可能有________种
(7)某苯的同系物的相对分子质量是92,在光照下,Cl2可以和其发生取代反应,取代产物的相对分子质量是126.5。写出该反应方程式_________________________________
(8)检验己烯中是否混有甲苯的试剂是________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物在生活、生产中有广泛应用。
(1)Na3AlF6是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上,用HF、Na2CO3和Al(OH)3制备冰晶石。化学反应原理是,2Al(OH)3+3Na2CO3+12H=2Na3AlF6+3CO2↑+9H2O.属于盐的有Na2CO3和_______。上述反应不能在玻璃容器中反应,其原因是________(用化学方程式表示)。
(2)明矾[KAl(SO4)2·12H2O]常作净水剂。在明矾溶液中滴加氢氧化钡溶液至Al3+恰好完全沉淀,写出该反应的离子方程式____________。
(3)铝合金广泛用于建筑材料。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生氢气体积相等(同温同压)。则该合金中铁、硅的质量之比为______。(已知:Si+2NaOH+H2O=Na2SiO3+ 2H2↑)
(4)铝氢化钠(NaAlH4)是有机合成的重要还原剂。它的制备方法是将氢化钠和氯化铝在乙醚中反应制备铝氢化钠。
①写出化学方程式________________。
②在化学上,含氢还原剂的还原能力用“有效氢”表示,”有效氢”含义是单位质量的含氢还原剂的还原能力相当于多少克氢气。一般地含氢还原剂的氢被氧化成H2O,“还原能力”用氢失去电子数多少表示。NaAlH4、NaH的“有效氢”之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给你提供纯锌、纯铜片和500 mL 0.4 mol·L-1的H2SO4溶液、导线、1000 mL量筒。试用下图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。

(1)如图所示,装置气密性良好,且1 000 mL量筒中已充满了水,则开始实验时,首先要______。
(2)a电极材料为________,其电极反应式为______________。b电极材料为________,其电极反应式为______________。
(3) 当量筒中收集672 mL气体时(已折算到标准状况下),通过导线的电子的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是重要的化工原料,用途非常广泛。
实验一:SO2可以抑制细菌滋生,具有防腐功效。某实验小组欲用下图所示装置测定某品牌葡萄酒中(葡萄酒中含有乙醇、有机酸等)的SO2含量。
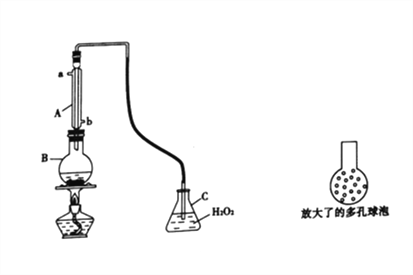
(1)仪器A的名称是________;使用该装置主要目的是____________________。
(2)B中加入 300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,C中化学方程式为_________________________________________。
(3)将输入C装置中的导管顶端改成具有多孔的球泡(如图15所示)。可提高实验的准确度,理由是_______________________________________。
(4)除去C中的H2O 然后用0.099mol·L-1NaOH标准溶液滴定。
①用碱式滴定管量取0.09mol·L-1NaOH标准溶液前的一步操作是___________________________;
②用该方法测定葡萄酒中SO2的含量偏高,主要原因是__________________________________,利用现有的装置,提出改进的措施是_______________________________________________。
(5)利用C中的溶液,有很多实验方案测定葡萄酒中SO2的含量。现有0.1mol·L-1BaCl2溶液,实验器材不限,简述实验步骤:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 由H2、碘蒸气、HI组成的平衡体系加压后颜色变深
B. 黄绿色的氯水光照后颜色变浅
C. 加压可使更多的SO2转化为SO3
D. 在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用三个集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量O2或Cl2,如图所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散)

(1)写出装置E中反应的离子方程式:__________________________________________
(2)假设该实验条件下,气体摩尔体积为aL·mol-1。则装置D的集气瓶中所得溶液溶质的物质的量浓度为____________;发生反应的方程式____________________________。
(3)通入氧气前在F装置的水槽里滴加几滴紫色石蕊溶液,观察到的现象是_____________,通入氧气后,可能观察到的实验现象是_________________________________________,写出反应的总化学方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Hf元素有多种核素,其中Hf是一种新合成的核素。下列关于![]() 的叙述中不正确的是( )
的叙述中不正确的是( )
A.该核素的质子数是72B.该核素的中子数是113
C.该核素的核外电子数是72D.该元素的相对原子质量是185
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com