
在一定温度下,某浓度的酸与金属锌反应生成NO2和NO,两者的物质的量之比为1: 3, 则要使I mol金属锌完全反应,反应过程中消耗HNO3的物质的量为
A.2.4 mol B.2.6 mol C.2.8 mol D.3.2 mol
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
美国天文学家认为在银河系中心2.6万光年处可能有乙醇醛糖分子存在。下列有关乙醇醛糖(HOCH2CHO)的说法中正确的是( )
A.乙醇醛糖是一种有机物,不易溶于水
B.乙醇醛糖能发生取代、消去、氧化以及中和反应
C.乙醇醛糖与甲酸甲酯互为同分异构体
D.将1 mol 乙醇醛糖与足量的银氨溶液作用,可析出1 mol Ag
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考二化学试卷(解析版) 题型:选择题
下列说法不正确的是 ( )
A.石油裂解和油脂皂化都是由高分子生成小分子的过程
B.丙烯分子中所有原子不可能在同一平面上
C.(CH3)3CCH2CH3的一氯代物有3种
D.甲苯的硝化、乙酸乙酯的水解均可看作取代反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42-、CO32-
B.在含大量Ba2+溶液中:NH4+、Na+、Cl-、OH-
C.在强碱溶液中:Na+、K+、Cl-、SO32-
D.在强酸性溶液中:K+、Fe2+、Cl-、CH3COO-
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期12月月考化学卷(解析版) 题型:实验题
高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如图),其实验流程如下:
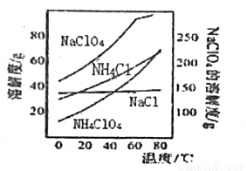
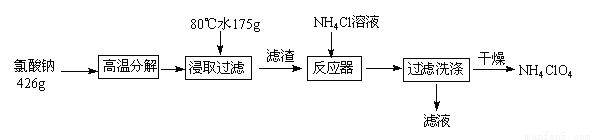
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为_______________。
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为_________________(写化学式)。
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为 _____________________。
(4)已知:2NH4ClO4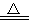 N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
A.饱和食盐水 B.浓H2SO4 C.NaOH溶液 D.Mg e.Cu f.Fe
利用下图装置对高氯酸铵热分解产生的三种气体进行分别吸收或收集。
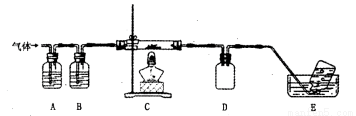
①E中收集到的气体可能是_______________________(填化学式)
②A、B、C中盛放的药品依次可以是__________(选填:“I”“II”“III”)。
I.abd II.cbe III.bcf
(5)过滤用到的主要玻璃仪器是____________________。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期12月月考化学卷(解析版) 题型:选择题
向盛有Cl2的六个集气瓶甲,乙、丙、丁、戊、己中各注入下列液体中的一种,经过震荡, 现象如下所示,则中、乙、丙、丁、戊、己中注入的液体分别是
①AgNO3溶液②NaOH溶液③水④淀粉-KI溶液⑤FeCl2与KSCN混合液⑥NaBr溶液
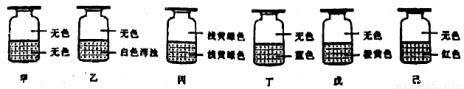
A.②①④⑥⑤③ B.②⑥①③④⑤ C.②⑥③④①⑤ D.②①③④⑥⑤
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期12月月考化学卷(解析版) 题型:选择题
从下列实验事实所列出的相应结论不正确的是
实 验事实 | 结 论 | |
① | SO2使酸性高猛酸钾溶液褪色 | 可证明SO2有漂白性 |
② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用硫磺粉处理洒落的金属汞 | 都发生了氧化还原反应 |
③ | 取少Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀,再滴加稀盐酸,沉淀不溶解 | 证明Na2SO3己氧化变质 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的气体,另取该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
⑤ | 在某溶液中加入适量新制饱和氯水,再加入CCl4震荡,CCl4层呈橙红色 | 该溶液一定有Br-存在 |
A.①③④ B.②③⑤ C.④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上12月考前测试化学卷(解析版) 题型:选择题
下列我国古代的技术应用中,其工作原理 不涉及化学反应的是( )
不涉及化学反应的是( )
A.火药使用 | B.粮食酿酒 | C.转轮 | D.铁的冶炼 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2016-2017学年海南省高一上期中化学试卷(解析版) 题型:实验题

(1)该浓盐酸中HCl的物质的量浓度为 mol•L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.400 mol•L-1的稀盐酸。
①容量瓶上需标有以下五项中的
A温度 B浓度 C容量 D压强 E刻度线
②将下列操作填写完整,并排列其正确的操作顺序(用字母表示,每个字母只能用一次) ;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡。
B.用量筒准确量取浓盐酸 mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。
C.将已冷却的盐酸沿玻璃杯注入 中。
D.将容量瓶盖紧,颠倒摇匀。
E.改用 加水,使溶液凹液面恰好与刻度相切。
F.继续往容量瓶内小心加水,直到液面接近刻度 处。
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”、“偏小”、“无影响”)。
Ⅰ 用量筒量取浓盐酸时俯视观察凹液面
Ⅱ 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
Ⅲ 定容时仰视刻度线
Ⅳ 溶液注入容量瓶前没有冷却至室温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com