
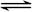 2HBr(g),能说明反应已达平衡状态的是 ( )
2HBr(g),能说明反应已达平衡状态的是 ( )| A.容器内混合气体颜色不随时间改变而改变 | B.H2、Br2的反应速率相等 |
| C.容器内的压强不随时间改变而改变 | D.混合气体的密度不随时间改变而改变 |
科目:高中化学 来源:不详 题型:单选题

A.c0 (g)+H (g)+H (g) (g)  F=e=CO(g)+H F=e=CO(g)+H 0(g)△H>0 0(g)△H>0 |
B.CH CH CH 0H(g) 0H(g)  CH CH =CH =CH (g)+H (g)+H 0(g)△H>0 0(g)△H>0 |
C.2C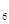 H H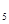 CH CH CH CH (g)+0 (g)+0 (g) (g)  2C 2C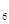 H H CH=CH CH=CH (g)+2H (g)+2H O(g)△H<0 O(g)△H<0 |
D.C0 (g)+2NH (g)+2NH (g) (g)  CO(NH CO(NH ) ) (s)+H (s)+H 0(g)△H<0 0(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
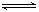 2Z(g)达化学平衡状态的标志是
2Z(g)达化学平衡状态的标志是| A.Z的生成速率与Z的分解速率相等 |
| B.单位时间生成amolX,同时生成3a molY |
| C.X、Y、Z的浓度相等 |
| D.X、Y、Z的分子数比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g),A的含量和温度的关系如图所示,下列结论正确的是:
C(g),A的含量和温度的关系如图所示,下列结论正确的是:
| A.T1>T2, 正反应吸热 | B.T1<T2, 正反应吸热 |
| C.T1>T2, 正反应放热 | D.T1<T2, 正反应放热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
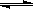 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
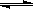 2NO(g)达到平衡时NO的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时NO的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字) C(g)+D(g),不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题: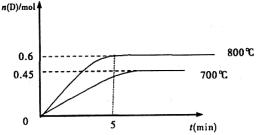
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z ,达到平衡后, X的转化率不可能为
2Z ,达到平衡后, X的转化率不可能为| A.25% | B.20% | C.15% | D.10% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 x Z(g) ΔH<0
x Z(g) ΔH<0| 恒容容器甲 | 恒容容器乙 | 恒压容器丙 | |
| 反应物投入量 | 3 mol X 1 mol Y | 1.2 mol X 0.4 mol Y 1.2 mol Z | 3 mol X 1 mol Y |
| X的浓度(mol·L―1) | c1 | c2 | c3 |
| Z的体积分数 | φ1 | φ2 | φ3 |
| 体系压强(Pa) | p1 | p2 | p3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。请根据图示回答下列问题:
。请根据图示回答下列问题: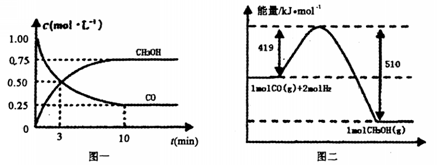
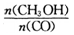 增大的有________________
增大的有________________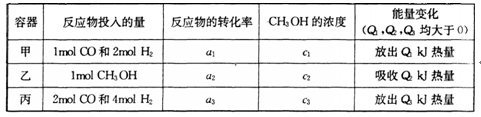
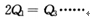
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com