
| A. | A2BC3 | B. | A4BC4 | C. | ABC4 | D. | A4B2C2 |
分析 有A、B、C三种短周期元素,A元素的原子半径是周期表中最小的元素,则A为H元素;B元素的原子最外层电子数为4,则B为碳或Si元素;C元素的原子最外层电子数次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素,结合常见化合物及元素化合价进行分析解答.
解答 解:有A、B、C三种短周期元素,A元素的原子半径是周期表中最小的元素,则A为H元素;B元素的原子最外层电子数为4,则B为碳或Si元素;C元素的原子最外层电子数次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素.
A.可以形成H2CO3或H2SiO3,故A正确;
B.可以形成H4SiO4,故B正确;
C.ABC4中B的化合价为+7,则B的最高化合价为+4,故C错误;
D.可以形成HOOC-COOH,故D正确,
故选C.
点评 本题考查了元素位置结构关系的应用,难度中等,能正确判断元素是解本题的关键,注意利用列举法解答.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:选择题
| A. | 用玉米、植物秸杆等作原料制造乙醇,用作汽车的燃料 | |
| B. | 用动物的骨或皮作原料制造中药,用作滋补品 | |
| C. | 用淀粉作原料提取淀粉酶,用作催化剂 | |
| D. | 用植物油或动物脂肪作原料制造人造金刚石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | (1)中红综色变深,(2)中红棕色变浅 | B. | (1)中红综色变浅,(2)中红棕色变深 | ||
| C. | 烧瓶(1)中气体的压强不变 | D. | 烧瓶(2)中气体的压强增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 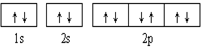 可表示单核10电子粒子基态时电子排布 可表示单核10电子粒子基态时电子排布 | |
| B. | 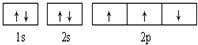 此图错误,违背了泡利原理 此图错误,违背了泡利原理 | |
| C. | 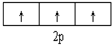 表示基态N原子的价电子排布 表示基态N原子的价电子排布 | |
| D. |  表示处于激发态的B的电子排布图 表示处于激发态的B的电子排布图 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
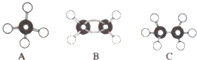
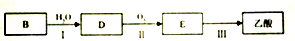
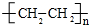
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.
高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 300 | 500 | 830 |
| 平衡常数K | 12 | 9 | 1 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图1中a~f分别表示有H、C、N、Na、Si、Cu元素组成的单质,其中c、d均是热和电的良导体,单质分别对应的熔点如图所示:
图1中a~f分别表示有H、C、N、Na、Si、Cu元素组成的单质,其中c、d均是热和电的良导体,单质分别对应的熔点如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com