
【题目】下列各种关于酸的使用,其中正确的是
A. 为了抑制Fe2+的水解,用稀硝酸酸化 B. 检验溶液中是否含有SO![]() 时,先用盐酸酸化
时,先用盐酸酸化
C. 乙酸与乙醇的酯化反应中,浓硫酸起到了催化剂和脱水剂的作用 D. 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在化工生产、污水处理等领域应用广泛。
(1)煤制得的化工原料气中含有羰基硫(O=C=S),该物质可转化为H2S,主要反应如下:
i.水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1
H2S(g)+CO2(g) △H1
ii.氢解反应:COS(g)+H2(g)![]() H2S(g)+CO(g) △H2
H2S(g)+CO(g) △H2
已知反应中相关的化学键键能数据如下表:

①恒温恒压下,密闭容器中发生反应i。下列事实能说明反应i达到平衡状态的是_______。(填标号)
a.容器的体积不再改变 b.化学平衡常数不再改变 c.混合气体的密度不再改变 d.形成1molH—O键,同时形成1molH—S键

②一定条件下,密闭容器中发生反应i,其中COS(g)的平衡转化率(α)与温度(T)的关系如图所示。则A、B、C三点对应的状态中,v(COS)=v(H2S)的是____________。(填标号)

③反应ii的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中 表示逆反应的平衡常数(K逆)的是__________(填“A”或“B”)。T1℃时,向容积为10L的恒容密闭容器中充入2molCOS(g)和1molH2(g),发生反应ii,CO的平衡转化率为___________。
(2)过二硫酸是一种强氧化性酸,其结构式为
①Ag+催化下,S2O82-与Mn2+在水溶液中生成SO42-和MnO4-,该反应离子方程式____________。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液的方法制备过二硫酸铵。总反应的离子方程式为____________________________________。
(3)NaHS可用于污水处理的沉淀剂。已知:25℃时,反应Hg2+(aq)+HS-(aq)HgS(s)+H+(aq)的平衡常数K=1.75×1038,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15。
①NaHS的电子式为____________________。
②Ksp(HgS)=_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源A 极的名称是_____________。
(2)甲装置中电解反应的总化学方程式是____________。
(3)如果收集乙装置中产生的气体,两种气体的体积比是____________(相同状况下)。
(4)欲用丙装置精炼铜,G应该是________(填“纯铜”或“粗铜”),精炼液的成分是__________。
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素有多种氧化物。请回答下列问题:
(1)已知:H2的燃烧热ΔH为-285.8kJ·mol-1。
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(1) ΔH=-44kJ·mol-1
则4H2(g) + 2NO2(g) = 4H2O(g) + N2(g) ΔH=__________。
(2)一定温度下,向2L恒容密闭容器中充入0.40mol N2O4,发生反应:N2O4(g)![]() 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/(mol·L-1) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①0-40s内,v(NO2)=________mol·L-1·s-1。
②升高温度时,气体颜色加深,则上述反应是________(填“放热”或“吸热”)反应。
③该温度下反应的化学平衡常数K=________mol·L-1。
④相同温度下,若开始向该容器中充入0.80molN2O4,则达到平衡后c(NO2)________ (填“>”“=”或“<”)0.60mol·L-1。
(3)N2O5是绿色硝化试剂,溶于水可得硝酸。下图是以N2O4为原料电解制备N2O5的装置。写出阳极区生成N2O5的电极反应式(注意阳极区为无水环境,HNO3亦无法电离):________________________。

(4)湿法吸收工业尾气中的NO2,常选用烧碱溶液,产物为两种常见的含氧酸盐。该反应的离子方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用下列试剂中的一种就能鉴别Ba(NO3)2、Na2CO3、KCl三种溶液,该试剂是( )
A. Ca(NO3)2溶液 B. 稀H2SO4 C. NaOH溶液 D. Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
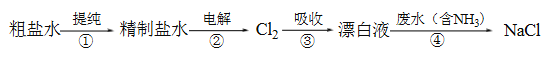
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然铊有两种稳定同位素![]() Tl和
Tl和![]() Tl。下列有关铊的同位素说法中,不正确的是( )
Tl。下列有关铊的同位素说法中,不正确的是( )
A. ![]() Tl和
Tl和![]() Tl质子数相同B.
Tl质子数相同B. ![]() Tl和
Tl和![]() Tl互为同素异形体
Tl互为同素异形体
C. ![]() Tl和
Tl和![]() Tl中子数之差为2D.
Tl中子数之差为2D. ![]() Tl原子核内中子数与核外电子数之差为43
Tl原子核内中子数与核外电子数之差为43
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com