
| A. | ①②③④⑤⑥ | B. | ④⑥ | C. | ②⑤⑥ | D. | ②⑤ |
分析 ①由两种或以上物质构成的是混合物;
②在水溶液中或熔融状态下能导电的化合物为电解质;
③能和碱反应生成盐和水的氧化物为酸性氧化物;
④同种元素的不同种单质间互为同位素;
⑤同种元素形成的不同种单质互为同素异形体;
⑥在溶液中和熔融状态下均不能导电的化合物为非电解质.
解答 解:①由两种或以上物质构成的是混合物,而水银是单质汞,为纯净物,故错误;
②在水溶液中或熔融状态下能导电的化合物为电解质,明矾、冰醋酸和石膏在水溶液中或熔融状态下均能导电,故为电解质,故正确;
③能和碱反应生成盐和水的氧化物为酸性氧化物,而氧化铝是两性氧化物,故错误;
④同种元素的不同种单质间互为同位素,而2H2不是原子是单质,故和其它两种不互为同位素,故错误;
⑤C60、金刚石、石墨是碳元素形成的不同种单质,故互为同素异形体,故正确;
⑥在溶液中和熔融状态下均不能导电的化合物为非电解质,而液氯即氯气为单质,故不是非电解质,故错误.
故选D.
点评 本题考查了电解质非电解质、纯净物混合物和同位素同素异形体等概念的辨别,把握住概念的要点是关键,难度不大.


科目:高中化学 来源: 题型:选择题
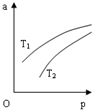 在密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ•mol-1,NH3 在 平衡混合气体中的体积分数(a)与温度(T)、压强(p)的关系如图所示.下列判 断正确的是( )
在密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ•mol-1,NH3 在 平衡混合气体中的体积分数(a)与温度(T)、压强(p)的关系如图所示.下列判 断正确的是( )| A. | T1>T2 | |
| B. | 其他条件不变,增大压强,可提高单位时间内 NH3的产量 | |
| C. | 升高温度,该反应的化学平衡常数增大 | |
| D. | 当 n(N2):n(H2):n(NH3)=1:3:2 时,反应一定达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用25 mL量筒量取12.36 mL盐酸 | |
| B. | 用pH试纸测出某溶液pH为3.5 | |
| C. | 用托盘天平称取8.75 g食盐 | |
| D. | 用酸式滴定管测出消耗盐酸的体积为15.60 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| B. | 4.4g二氧化碳气体中所含的原子个数与4.2g氮气中所含的原子个数不相等 | |
| C. | 常温常压下,11.2LNH3所含的原子数目为2NA | |
| D. | 常温常压下,48gO3含有的氧原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

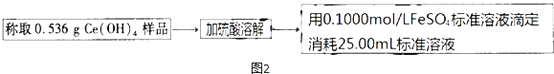
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{还原}^{H_{2}}$Si | |
| B. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| C. | FeS2$→_{还原}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| D. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com