
某温度下在容积固定的密闭容器中,下列反应达到平衡:
CO(g)+H2O(g) 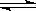 CO2(g)+H2(g)
CO2(g)+H2(g)
| 初始投料比n(CO)n(H2O) | CO转化率 | H2O转化率 |
| 1:1 | 0.5 | 0.5 |
| 1:2 | 0.67 | 0.335 |
| 1:3 | 0.75 | 0.25 |
(1)已知CO和H2的燃烧热分别为283kJ/mol、285.8kJ/mol,H2O(g)=H2O(l)△H= -44kJ/mol,写出CO(g)和H2O(g)反应的热化学方程式 。
(2)该反应的平衡常数为 。该温度下,向该容器中充入1mol CO、3molH2O(g)、2mol CO2、1.5molH2,则起始时该反应速率V正 V逆(填“>”、“<”或“=”)
(3)结合表中数据判断下列说法中正确的是 。
A.增加H2O(g)的量,CO的转化率升高而H2O(g)的转化率降低
B.若CO与H2O(g)的转化率相同,则二者的初始投入量一定相同
C.CO和H2O(g)初始物质的量之比等于二者转化率之比
D.当CO与H2O(g)物质的量之比为1:4时,CO的转化率为0.85
【答案】(1)CO(g)+H2O(g)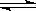 CO2(g)+H2(g)△H=-41.2kJ/mol(2)1 ; = ;(3) AB
CO2(g)+H2(g)△H=-41.2kJ/mol(2)1 ; = ;(3) AB
【解析】
试题分析:(1)已知CO和H2的燃烧热分别为283kJ/mol、285.8kJ/mol,则CO(g)+1/2O2(g)=CO2(g)△H=-283kJ/mol;H2(g)+1/2O2(g)=H2O(l)△H=-285.8kJ/mol;H2O(g)=H2O(l)△H= -44kJ/mol,①式+③式-②式得CO(g)+H2O(g)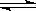 CO2(g)+H2(g)△H=-41.2kJ/mol,故答案为CO(g)+H2O(g)
CO2(g)+H2(g)△H=-41.2kJ/mol,故答案为CO(g)+H2O(g)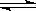 CO2(g)+H2(g)△H=-41.2kJ/mol(2)若初始投料比为11,则CO的转化率为0.5,平衡常数K=
CO2(g)+H2(g)△H=-41.2kJ/mol(2)若初始投料比为11,则CO的转化率为0.5,平衡常数K=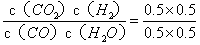 =1,向该容器中充入1mol CO、3molH2O(g)、2mol CO2、1.5molH2,,则Qc=
=1,向该容器中充入1mol CO、3molH2O(g)、2mol CO2、1.5molH2,,则Qc=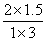 =1,V正=V逆.(3)A.增加H2O(g)的量,是平衡向正反应方向移动,CO的转化率增大,水的转化率降低,A正确;B.CO与H2O(g)的计量数相等,若CO与H2O(g)的转化率相同,则二者的初始投入量一定相同,B正确;CO和H2O(g)始终按照系数比转化,即按照11进行转化,但初始的物质的量不一定按11进行投料,C错误;CO(g)+H2O(g)
=1,V正=V逆.(3)A.增加H2O(g)的量,是平衡向正反应方向移动,CO的转化率增大,水的转化率降低,A正确;B.CO与H2O(g)的计量数相等,若CO与H2O(g)的转化率相同,则二者的初始投入量一定相同,B正确;CO和H2O(g)始终按照系数比转化,即按照11进行转化,但初始的物质的量不一定按11进行投料,C错误;CO(g)+H2O(g)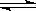 CO2(g)+H2(g)假设一氧化碳转化率为x,则CO转了xmol,二氧化碳和氢气分别生成(1-x),由平衡常数K=1=
CO2(g)+H2(g)假设一氧化碳转化率为x,则CO转了xmol,二氧化碳和氢气分别生成(1-x),由平衡常数K=1=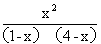 ,解得x=0.8,即转化率为80%,D错误;答案选AB.
,解得x=0.8,即转化率为80%,D错误;答案选AB.
考点:化学平衡常数的有关计算


科目:高中化学 来源: 题型:
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe (s)+3CO(g) ΔH 1=+489.0 kJ· mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1, 则CO还原Fe2O3(s)的热化学方程式为 。
(2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 。
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g)  CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
|

①该反应的ΔH 0(填“大于或小于”),曲线I、Ⅱ对应的平衡常数大小关系为
KⅠ KⅡ (填“>、=或<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2、3 mol H2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为 。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 (填序号)。
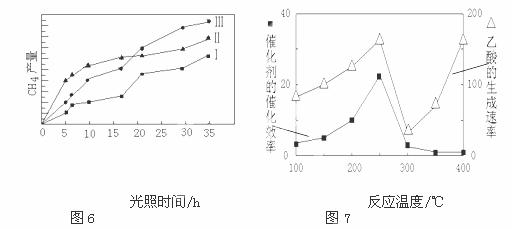
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图7。
①当温度在 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数,下列说法中正确的是( )
A.2.9 g 2CaSO4·H2O中含有的结晶水分子数为0.02NA
B.30 g乙酸和葡萄糖的混合物中含碳原子数为NA
C.在铁与硫的反应中,1 mol铁失去的电子数为3NA
D.62 g Na2O溶于水后所得溶液中含有的O2-数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在平衡:2CrO42-(黄色)+2H+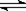 Cr2O72-(橙红色)+H2O中,溶液颜色介于黄色和橙红色之间。若使溶液的橙红色加深,则应向溶液中加入的是
Cr2O72-(橙红色)+H2O中,溶液颜色介于黄色和橙红色之间。若使溶液的橙红色加深,则应向溶液中加入的是
A.少量浓硫酸 B.少量氢氧化钠固体 C.少量氯化钾固体 D.少量H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2SO2 (g) + O2 (g) 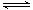 2SO3 (g) ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2 (乙) 1 mol SO2和0.5 mol O2 (丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g) ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2 (乙) 1 mol SO2和0.5 mol O2 (丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙 > 2P乙
B.SO3的质量m:m甲=m丙 > 2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙 > 2Q乙
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的离子方程式正确的是 ( )
A.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
B.铁溶于稀硝酸,溶液变黄:3Fe +8H+ +2NO3-=3Fe2++2NO↑+4H2O
C.向NaAlO2溶液中通入过量的CO2:CO2+ 2AlO2- + 3H2O =2Al(OH)3 ↓ + CO32-
D.用小苏打治疗胃酸过多:HCO3-+H+ = CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com