


科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①③②④ | B.①②③④ |
| C.①④③② | D.①③④② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | | | ② | ④ | |
| 3 | ⑤ | | ③ | | | ⑥ | ⑦ | |
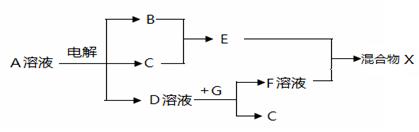
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径逐渐增大 | B.单质的氧化性逐渐增强 |
| C.单质熔、沸点逐渐降低 | D.气态氢化物稳定性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. | B. |
C. | D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该元素属于第七周期 | B.该元素位于ⅢA族 |
| C.该元素为金属元素,性质与82Pb相似 | D.该同位素原子含有114个电子,184个中子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com