
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2
乙:MgO、NO2、O2
丙:Mg3N2、O2
丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是 。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
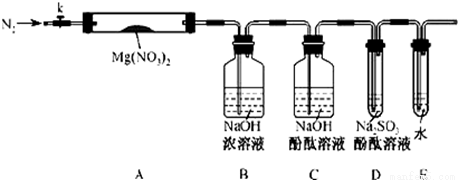
(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明 。
②称取Mg(NO3)2固体3.79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是 ;关闭K,用酒精灯加热时,正确操作是先 然后固定在管中固体部位下加热。
③观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想 是正确的。
②根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应: (填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是 。
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
(1)不符合氧化还原反应原理
(2)①装置气密性良好
②避免对产物O2检验产生干扰;移动酒精灯预热硬质玻璃管
(3)①乙 ②2Na2SO3+O2=2Na2SO4;O2在通过装置B时已参与反应
【解析】(1)由于产物中N化合价只有降低情况,没有升高,故答案为:不符合氧化还原反应原理(或其它合理答案);
(2)①实验前需要检验装置的气密性,方法是关闭k,微热硬质玻璃管(A),观察到E中有气泡连续放出,证明装置气密性良好,故答案为:装置气密性良好;②由于甲乙丙猜想中产物都有氧气,没有氮气,用氮气排出装置中空气避免对产物氧气检验的干扰,集中加热前先预热硬质试管,然后固定在管中固体部位下加热,故答案为:避免对产物O2检验产生干扰(或其它合理答案);移动酒精灯预热硬质玻璃管;(3)①硝酸镁分解,红棕色气体是二氧化氮,镁元素不会还是硝酸镁形式,所以乙正确;故答案为:乙;②亚硫酸钠和氧气的反应,反应方程式是:2Na2SO3+O2=2Na2SO4,在B装置中,二氧化氮和氢氧化钠溶液反应生成一氧化氮,生成的一氧化氮消耗了氧气,故答案为:2Na2SO3+O2=2Na2SO4;O2在通过装置B时已参与反应。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014高考名师推荐化学电解三池的应用(解析版) 题型:选择题
如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是
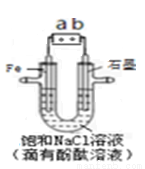
A.a 为电源的正极
B.通电一段时间后,石墨电极附近溶液先变红
C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑
D.电解饱和食盐水的总反应是: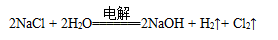
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学物质的量及相关计算(解析版) 题型:选择题
下列叙述正确的是
A.1 mol·L-1NaCl溶液含有NA个Na+
B.10 mL质量分数为98%的H2SO4用水稀释至100 mL,H2SO4的质量分数应大于9.8%
C.配制240 mL 1 mol·L-1的NaOH溶液需称NaOH固体的质量为9.6 g
D.配制1 mol·L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学物质的检验(解析版) 题型:选择题
下列实验设计能够成功的是
A.检验亚硫酸钠试样是否变质:

B.除去粗盐中含有的硫酸钙杂质

C.检验某溶液中是否含有Fe2+

D.证明酸性条件H2O2的氧化性比I2强:

查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学物质的分离和提纯(解析版) 题型:选择题
用下列实验装置进行相应的实验,能达到实验目的的是
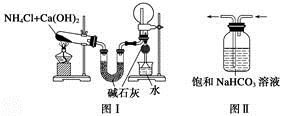
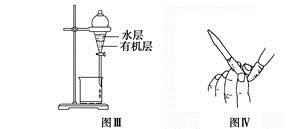
A.图Ⅰ用于实验室制氨气并收集干燥的氨气
B.图Ⅱ用于除去CO2中含有的少量HCl
C.图Ⅲ用于提取I2的CCl4溶液中的I2
D.图Ⅳ用于检查碱式滴定管是否漏液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学燃烧热与盖斯定律(解析版) 题型:选择题
已知1 g氢气完全燃烧生成液态水时放出热量143 kJ,18 g水蒸气变成液态水放出44kJ的热量。其它相关数据如下表,则表中X为:
| O=O(g) | H-H(g) | H-O(g) |
1mol化学键断裂时需要吸收的能量/kJ | 496 | X | 463 |
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学热化学方程式的正误判断及书写(解析版) 题型:选择题
已知:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.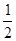 H2SO4(aq)+
H2SO4(aq)+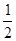 Ba(OH)2(aq)===
Ba(OH)2(aq)===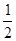 BaSO4(s)+H2O(l)ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l)ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学水的电离与溶液酸碱性(解析版) 题型:选择题
250C时,pH=3的HNO3,下列该硝酸说法正确的是
A.该硝酸中水电离出的c(H+)=1.0×10-3mol/L
B.加水稀释到原溶液体积的100倍,硝酸溶液的pH为5
C.相同温度下,pH=3的CH3COOH溶液的物质的量浓度与该硝酸相同
D.该硝酸中加入少量的Zn粒产生H2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原规律(解析版) 题型:选择题
已知电离平衡常数:H2CO3>HClO>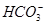 ,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是
,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是
A.向FeI2溶液中滴加少量氯水,离子方程式为2Fe2++Cl2=2Fe3++2Cl-
B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色
C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32-
D.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com