
【题目】下图是三种稀酸对![]() 合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是
合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是

A.稀硝酸对![]() 合金的腐蚀性比稀硫酸和稀盐酸的弱
合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是:Fe+6HNO3(稀)![]() Fe(NO3)3+3NO2↑+3H2O
Fe(NO3)3+3NO2↑+3H2O
C.Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对![]() 合金的腐蚀性最强
合金的腐蚀性最强
D.随着Cr含量增加,稀硝酸对![]() 合金的腐蚀性减弱
合金的腐蚀性减弱
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知:反应aA(g)+bB(g)cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。

(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为___________________,该反应的化学方程式为______________________。
(2)经12s时间,v(A)=___________,v(C)=___________,该反应12s时___________达到化学平衡(“是”或“否”)。
Ⅱ.(3)下列说法可以证明H2(g)+I2(g)2HI(g)已达平衡状态的是________(填序号)。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示。若关闭阀门Ⅰ,打开阀门Ⅱ,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭阀门Ⅱ,打开阀门Ⅰ,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
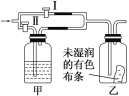
①浓硫酸 ②饱和氯化钠溶液 ③亚硫酸钠溶液 ④饱和碳酸氢钠溶液
A.①②③B.②③④
C.①②④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组模拟工业生产制取HNO3设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。请回答下列问题。
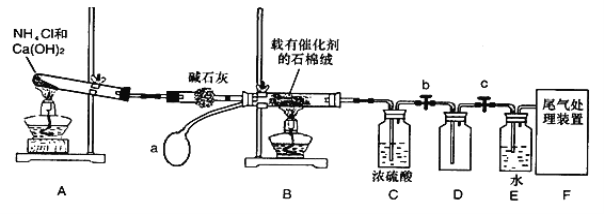
(1)写出装置B中主要反应的化学方程式 ________________________。
(2)装置E中主要反应的化学方程式______________________________。
(3)装置C中浓硫酸的作用是________________________________。
(4)请你帮助该化学小组设计实验室制取NH3的另一方案_________________________。
(5)装置D中的主要作用是 _______________________。
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计下图所示装置(仪器固定装置省略,挤出气体的气球紧套在玻璃管一端,玻璃管插在单孔橡胶塞上)进行验证。实验步骤如下:
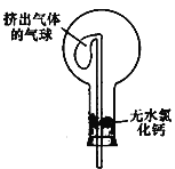
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是______,由此,该同学得出结论:不能用CaCl2代替碱石灰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上通过高温分解FeSO4的方法制备Fe2O3,化学方程式为:2FeSO4 ![]() Fe2O3+ SO3↑ + SO2↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO3↑ + SO2↑为检验FeSO4高温分解的产物,进行如下实验:
检验FeSO4高温分解产生的气体,将FeSO4高温分解产生的气体通入下图装置中。
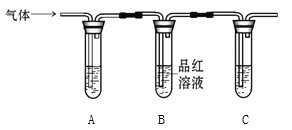
① 装置A试管可选用的试剂是_________(填标号)。
a. 水 b. BaCl2溶液 c. Ba(NO3)2溶液 d. Ba(OH)2溶液
② 装置C的作用是防止尾气污染环境,试管中应加入的试剂是_________________。
③ 若装置B试管中溶液改为酸性KMnO4溶液,可以观察到溶液紫色褪去,反应的离子方程式为__________________________ 。
(2)工业上在一定温度和催化剂条件下用NH3将NO2还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。

①实验室可以用A、B或C装置制取氨气,如果用C装置,则该装置中烧瓶所盛放的试剂为________(写名称);反应的化学方程式是_____________________;
② 预收集一瓶干燥的氨气,选择下图中的装置,其气体收集和尾气处理装置连接顺序依次为:发生装置→_____________________(用字母表示)

③ 将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管观察到的实验现象是____________________ ,反应的化学方程式为 ______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx(主要指NO和NO2)是大气主要污染物之一,有效去除大气中的NOx是环境保护的重要课题。可以利用NH3与NOx反应消除NOx。
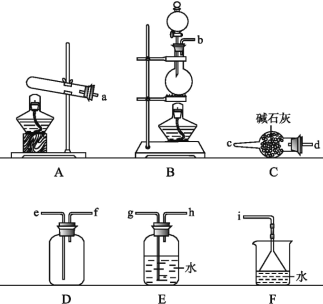
(1)实验室制取NH3,发生装置可以选择上图中的____________,反应的化学方程式为____________。
(2)欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→____________(按气流方向,用小写字母表示)。
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。NH3与NO2生成N2的反应中,当生成1molN2时,转移电子的物质的量为____________mol。
(4)用酸性(NH2)2CO水溶液也可以吸收NOx,吸收过程中存在HNO2与CO(NH2)2生成N2和CO2的反应。该反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是( )
A.用20mL量筒量取15mL 酒精,加水5mL,配制质量分数为75%酒精溶液
B.在200mL 某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属阳离子,不考虑水解问题,则该硫酸盐的物质的量浓度为2.5mol·L1
C.实验中需用2.0mol·L1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为 1000mL、201.4g
D.实验室配制500mL0.2mol·L1的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾(FeSO4·7H2O),放入小烧杯中加水溶解,转移到500mL容量瓶,洗涤、稀释、定容、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.由铜、锌作电极与硫酸溶液组成的原电池中,溶液中的H+向正极移动
B.钢铁发生腐蚀时,正极上发生的反应为Fe-2e-=Fe2+
C.铜锌原电池工作时,若有13 g锌被溶解,溶液中就有0.4 mol电子通过
D.原电池必须有两个活泼性不同的金属作电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Co(NH3)5BrSO4可形成两种钴的配合物,已知两种配合物的分子式分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br,分别向两种配合物的溶液中加BaCl2溶液,有白色沉淀产生的是_____。
(2)向CuSO4溶液中逐滴加入稀氨水,所得配合物的化学式为_____,该配合物中存在的化学键类型为_________。
(3)铁可形成多种配位化合物,但与氨形成的化合物不稳定,如FeCl2虽然可以与氨气形[Fe(NH3)6]Cl2,但此物质遇水即生成灰白色沉淀,写出对应的反应方程式:_____。[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体_____。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com