
| A. | 酸性:H2SiO3>H2CO3 | B. | 还原性:Na>Al | ||
| C. | 热稳定性:Na2CO3>NaHCO3 | D. | 熔点:SiO2>CO2 |
分析 A.非金属性越强,对应最高价氧化物的水化物的酸性越强;
B.金属性越强,对应单质的还原性越强;
C.碳酸盐比碳酸氢盐稳定;
D.熔点的一般规律:原子晶体>离子晶体>分子晶体.
解答 解:A.非金属性越强,对应最高价氧化物的水化物的酸性越强,非金属性:Si<C,酸性:H2SiO3<H2CO3,故A错误;
B.金属性越强,对应单质的还原性越强,金属性:Na>Al,则还原性:Na>Al,故B正确;
C.碳酸盐比碳酸氢盐稳定,则热稳定性:Na2CO3>NaHCO3,故C正确;
D.熔点的一般规律:原子晶体>离子晶体>分子晶体,SiO2属于原子晶体,CO2属于分子晶体,所以熔点:SiO2>CO2,故D正确.
故选A.
点评 本题考查金属性和非金属性、熔点等,明确物质的酸性、气态氢化物的稳定性,碱性与非金属性、金属性的关系是解答本题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 若C为固体,则B一定是气体 | |
| B. | B和C一定都是气体 | |
| C. | 若起始时往容器中投入18gA,则反应吸收的热量为44.5kJ | |
| D. | 若起始时往容器中投入18gA,则反应放出的热量为44.5kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
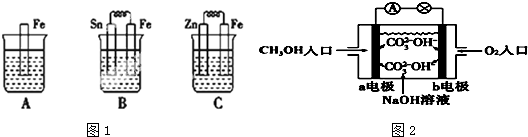
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖溶于水 | B. | 金刚石变成石墨 | C. | 氯化钠熔化 | D. | 水的汽化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与碘水混合振荡,水层颜色变浅发生萃取 | |
| B. | 乙烯使溴水褪色 | |
| C. | 甲烷与氯气光照下反应 | |
| D. | 乙烯与氯化氢在一定条件下反应制取纯净的一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径B>A>D | B. | 离子半径C>D>B>A | ||
| C. | 单质还原性A>B>D>C | D. | A、B、C、D可能是第二周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g CO和32g O2所具有的总能量大于88g CO2所具有的总能量 | |
| B. | CO不如 CO2稳定 | |
| C. | 12g C所具有的能量一定高于28g CO所具有的能量 | |
| D. | 将一定质量的炭燃烧,生成CO2比生成CO时放出的热量多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com