
有关元素X、Y、Z、D、E的信息如下:
| 有关信息 | |
| X | 元素主要化合价为-2,原子半径为0.074 nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102 nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物可溶于水,且能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
 请回答下列问题:
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为___________。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_______。
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2只能通过置换反应生成,EY3只能通过化合反应生成
③铜片、碳棒和EY3溶液组成原电 池,电子由铜片沿导线流向碳棒
池,电子由铜片沿导线流向碳棒
(3)将Z单质在X的单质中燃烧的产物和等物质的量的Y单质同时通入足量的水中,充分反应后的溶液中滴 入品红溶液,现象是__________________,有关反应的离子方程式为________________________________________________________________________。
入品红溶液,现象是__________________,有关反应的离子方程式为________________________________________________________________________。
解析:元素主要化合价为-2的X为氧元素;所在主族序数与所在周期序数之差为4的情况有两种,一是氧元素,二是氯元素,显然Y不可能再是氧,而是氯元素;单质在氧气中燃烧,发出明亮的蓝紫色火焰的Z是硫元素;最高价氧化物对应的水化物电离出电子数相等(各10个)的阴阳离子的是碱,该可溶性碱只能是NaOH,D是钠元素;在潮湿空气中易被腐蚀或损坏的常见金属为铁。
(1)氧的氢化物中可用于实验室制取O2的是H2O2,其化学方程式为2H2O2 2H2O+O2↑。
2H2O+O2↑。
(2)铁与氯可形成 两种化合物FeCl2、FeCl3, 保存FeCl2溶液时,需向溶液中加入少量Fe单质,防止Fe2+被氧化,①正确;FeCl2也可以通过化合反应生成,如2FeCl3+Fe===3FeCl2,②不正确;铜片、碳棒和FeCl3溶液组成的原电池中铜片为负极,电子由铜片沿导线流向碳棒,③正确。(3)SO2与Cl2等物质的量反应可生成不具有漂白性的HCl和H2SO4,反应后的溶液中滴入品红溶液,品红不褪色。
两种化合物FeCl2、FeCl3, 保存FeCl2溶液时,需向溶液中加入少量Fe单质,防止Fe2+被氧化,①正确;FeCl2也可以通过化合反应生成,如2FeCl3+Fe===3FeCl2,②不正确;铜片、碳棒和FeCl3溶液组成的原电池中铜片为负极,电子由铜片沿导线流向碳棒,③正确。(3)SO2与Cl2等物质的量反应可生成不具有漂白性的HCl和H2SO4,反应后的溶液中滴入品红溶液,品红不褪色。
答案:(1)2H2O2 2H2O+O2↑ (2)①、③
2H2O+O2↑ (2)①、③
(3)溶液呈红色且不褪去 SO2+Cl2+2H2O===4H++SO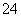 +2Cl-
+2Cl-


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列叙述中正确的是
( )
A.分子式相同,各元素百分含量也相同的物质是同种物质
B.化学性质相似的不同物质一定属于同系物
C.分子式相同而结构不同的物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
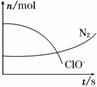 某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO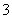 、N2、Cl-六种物质。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是( )
、N2、Cl-六种物质。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是( )
A.还原剂是含CN-的物质,氧化产物只有N2
B.氧化剂是ClO- , 还原产物是HCO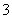
C.配平后氧化剂与还原剂的化学计量数之比为5∶2
D.若生成2.24 L N2(标准状况),则转移电子0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是( )
| X | Y | ||
| Z | W | Q |
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q弱
D.X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构相同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)2012年伦敦奥运会火炬采用丙烷为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
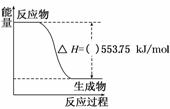
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”。
②写出表示丙烷燃烧热的热化学方程式:___________________________________。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________。
(2)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)===H2O(l) ΔH1=-Q1 kJ/mol C2H5OH(g)===C2H5OH(l) ΔH=-Q2 kJ/mol
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH3=-Q3 kJ/mol
若使46 g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为________kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+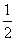 O2(g)===CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
O2(g)===CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃与氢气加成后得到2,2二甲基丁烷,该烃的名称可能是
( )
A.3,3二甲基1丁炔 B.2,2二甲基2丁烯
C.2,2二甲基1丁烯 D.3,3二甲基1丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx,可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
A.若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ
B.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH<-574 kJ·mol-1
C.反应①②转移的电子数相同
D.反应②中当4.48 L CH4反应完全时转移的电子总数为1.60 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com