
已知红磷通常要比白磷稳定,下列两个反应:
①P4(白磷、s)+5O2(g)===2P2O5(s) ΔH1
②4P(红磷、s)+5O2(g)===2P2O5(s) ΔH2
则ΔH1和ΔH2的关系是( )
A.ΔH1=ΔH2 B.ΔH1>ΔH2
C.ΔH1<ΔH2 D.无法确定
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列有机物的命名正确的是( )
A. 3,3-二甲基-4-乙基戊烷 B. 3,3,4-三甲基-1-己烯
C. 3,4,4-三甲基己烷 D. 2,3,3-三甲基-2-庚烯
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列元素的半径为:
| 原子 | N | S | O | Si |
| 半径r/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
根据以上数据,磷原子的半径可能是( )
A.1.10×10-10m B.0.80×10-10m C.1.20×10-10m D.0.70×10-10m
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素的原子核电荷数和中子数一定为6 ④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右图,则下列说法正确的是( )
A.阳极产物一定是Cl2,阴极产物一定是Cu
B.BC段表示在阴极上是H+放电产生了H2
C.整个过程中阳极先产生Cl2,后产生O2
D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是
 A.b代表0℃下CH3COCH3的Y-t 曲线
A.b代表0℃下CH3COCH3的Y-t 曲线
B.反应进行到20min末,CH3COCH3的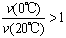
C.升温可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的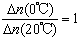
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)上图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式 ;写出该反应的化学平衡常数表达式K= ;降低温度,该反应的K值 。(填“增大”、“减小”或“不变”)
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能 kJ·mol-1
(3)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ;△H1= akJ·mol-1
N2(g)+O2(g) 2NO(g);△H2= bkJ/mol
 若1mol NH3还原NO生成N2,则该反应过程中的反应热△H3= kJ/mol(用含a、b的式子表示)
若1mol NH3还原NO生成N2,则该反应过程中的反应热△H3= kJ/mol(用含a、b的式子表示)
(4)肼(N2H4)在空气中燃烧的热化学方程式为
N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H= —534kJ/mol
肼-空气燃料电池是一种碱性电池,电解质溶液是20~30%的KOH溶液,如右图所示。
写出该电池的负极反应式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.氨气是非电解质,氨水是电解质
B.氢氧化铁胶体可以发生丁达尔现象
C.摩尔和物质的量均是联系宏观和微观数量的物理量
D.二氧化硅既可和酸又可和碱反应,所以二氧化硅是两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
铁镍蓄电池又称爱迪生电池,放电时的总反应为:
Fe+Ni2O3+3H2O==Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-==Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-==Ni2O3+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com