
【题目】下列说法中正确的是
A.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
B. 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质
C.铜、石墨均导电,所以它们是电解质
D.液态HCl、固态NaCl均不导电,所以HCl、NaCl均不是电解质
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO![]() )>c(NH
)>c(NH![]() )
)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016年北京Ⅰ卷】以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
2 mL | 0.2 mol·L1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
0.2 mol·L1 CuSO4溶液 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
0.1 mol·L1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ: 。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42,含有Cu+、Cu2+和SO32。已知:Cu+![]() Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是 。
②通过下列实验证实,沉淀中含有Cu2+和SO32。
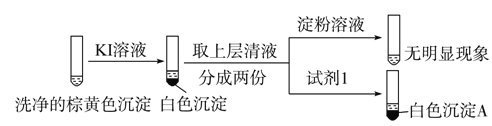
a.白色沉淀A是BaSO4,试剂1是 。
b.证实沉淀中含有Cu2+和SO32的理由是 _。
(3)已知:Al2(SO4)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和 。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
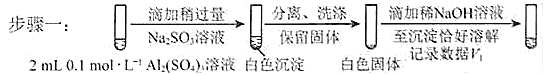
步骤二: (按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有 。盐溶液间反应的多样性与 有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将X和Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应:2X(g)+ Y(s)![]() 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表下列说法正确的是( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表下列说法正确的是( )
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.10 | 0.09 | 0.09 |
A.反应前2min的平均速率v(Z)=2.0×10-3 mol/(L·min)
B.其他条件不变,加入一定量的Y,反应速率一定加快
C.反应进行4s时,X的转化率75%
D.反应达到平衡时,X的物质的量浓度为0.02mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)==2SO3(g)反应过程中的能量变化如下图所示。
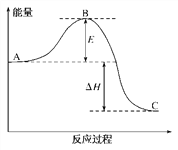
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示__________的能量、___________的能量;
(2)图中ΔH=______________________;
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=___________;
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷广泛应用于家用液化石油气及打火机中作燃料,下列关于丁烷叙述不正确的是( )
A. 常温下,C4H10是液体
B. C4H10和CH4互为同系物
C. 丁烷有正丁烷和异丁烷两种同分异构体
D. 丁烷在一定条件下与氯气发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(A类题)已知下列热化学方程式:
①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ
②C(s)+H2O(s)=CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
③![]() H2SO4(1)+NaOH(1)=
H2SO4(1)+NaOH(1)=![]() Na2SO4(1)+H2O(1) ΔH=-57.3 kJ·mol-1
Na2SO4(1)+H2O(1) ΔH=-57.3 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
⑤CO(g)+![]() O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(1) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(1) ΔH=-517.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有 ,不正确的理由分别是 。
(2)根据上述信息,写出C转化为CO的热化学方程式:_______________。
(3)上述反应中,表示燃烧热的热化学方程式有 ;表示中和热的热化学方程式有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 焓变和熵变都大于0的反应肯定是自发的
B. 焓变小于0而熵变大于0的反应肯定是自发的
C. 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D. 在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是

A. 原子半径:Y>Z>W
B. 单质的还原性:X>Y
C. 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D. 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com