
| A. | 纯碱溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| B. | 醋酸溶液显酸性:CH3COOH+H2O?CH3COO-+H3O+ | |
| C. | 向碘化亚铁溶液中通入足量的溴水:3Br2+2Fe2++4I-═6Br-+2Fe3++2I2 | |
| D. | 向碳酸氢钙溶液中滴加过量的烧碱溶液:HCO3-+Ca2++2OH-═CaCO3↓+H2O |
分析 A.碳酸根离子的水解分步进行,主要以第一步为主,离子方程式写出第一步水解的反应即可;
B.醋酸为弱电解质,在溶液中部分电离,存在电离平衡;
C.溴水足量,亚铁离子和溴离子完全反应;
D.氢氧化钠过量,反应生成碳酸钙沉淀、碳酸钠和水.
解答 解:A.纯碱溶液显碱性,碳酸根离子的水解分步进行,离子方程式写出第一步即可,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故A错误;
B.醋酸为弱酸,在溶液中部分电离,其电离方程式为:CH3COOH+H2O?CH3COO-+H3O+,故B正确;
C.向碘化亚铁溶液中通入足量的溴水,反应生成溴化铁和碘单质,反应的离子方程式为:3Br2+2Fe2++4I-═6Br-+2Fe3++2I2,故C正确;
D.碳酸氢钙溶液中滴加过量的烧碱溶液,反应生成碳酸钠、碳酸钙沉淀和水,正确的离子方程式为:2HCO3-+Ca2++2OH-═CO32-+CaCO3↓+2H2O,故D错误;
故选BC.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学卷(解析版) 题型:选择题
在电解水制取H2和O2时,为了增强导电性,常常在水中加入一些电解质,下列物质可选用
A.NaCl B.CuCl2 C.NaOH D.CuSO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
下列说法正确的是
A.同温、同压下,相同质量的气体都占有相同的体积
B.同温、同压下,相同体积的气体都含有相同数目的原子
C.在任何情况下,1molCO2和64gSO2所含有分子数和原子总数都相同
D.1mol某气体的体积约为22.4L,该气体所处的情况一定是标准状况
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
下列实验操作中错误的是
A.进行蒸发操作时,蒸发皿中出现大量固体时,即可停止加热
B.进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
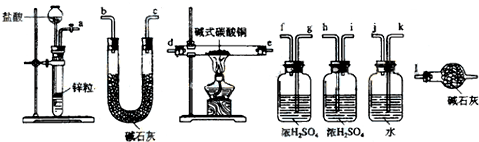
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
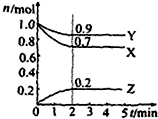 某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
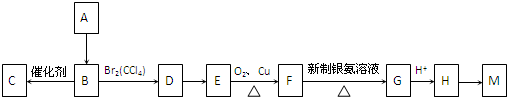
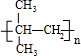 ,M的结构简式为
,M的结构简式为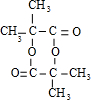 .
.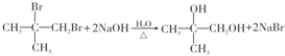 ;
;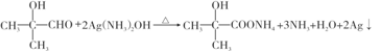 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不能使酸性高锰酸钾溶液褪色 | B. | 苯的一氯代物只有一种 | ||
| C. | 苯的二氯代物只有三种 | D. | 苯分子中六个碳碳键键长完全相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com