
 某同学利用如图所示实验装置测定常温常压下的气体摩尔体积.
某同学利用如图所示实验装置测定常温常压下的气体摩尔体积.分析 (1)由图可知仪器的名称,利用气体的压强使液体顺利流下;
(2)记录量气管读数时,在常温下进行,且调节液面相平;
(3)Mg~H2↑,气体的物质的量等于Mg的物质的量,均为$\frac{0.048g}{24g/mol}$=0.002mol,气体体积为49.60mL-0.10mL=49.50mL,结合Vm=$\frac{V}{n}$计算;测定结果比理论值偏大,则气体体积偏大;
(4)用装置B代替装置A,实验精确度更高,可避免液体体积对实验的影响.
解答 解:(1)仪器a的名称为锥形瓶,通过分液漏斗向仪器a中加入硫酸溶液的操作是 将分液漏斗玻璃塞上的凹槽与漏斗口颈上的小孔对准(或将玻璃塞拔开),缓慢旋转分液漏斗的旋塞,使硫酸溶液缓慢流入锥形瓶,适时关闭旋塞,
故答案为:锥形瓶;将分液漏斗玻璃塞上的凹槽与漏斗口颈上的小孔对准(或将玻璃塞拔开),缓慢旋转分液漏斗的旋塞,使硫酸溶液缓慢流入锥形瓶,适时关闭旋塞;
(2)在记录量气管读数时,应注意将装置冷却至室温,再调节水准管高度,使其液面与量气管中液面相平,视线与量气管内凹液面相切,水平读数,
故答案为:装置冷却至室温;调节水准管高度,使其液面与量气管中液面相平;
(3)Mg~H2↑,气体的物质的量等于Mg的物质的量,均为$\frac{0.048g}{24g/mol}$=0.002mol,气体体积为49.60mL-0.10mL=49.50mL,此条件下气体摩尔体积为$\frac{0.0495L}{0.002mol}$=24.75 L•mol-1; 测定结果比理论值偏大,则气体体积偏大,b、c均符合,
故答案为:24.75 L•mol-1;bc;
(4)与原方案装置相比,有同学设想用装置B代替装置A,实验精确度更高.理由为避免加入硫酸时,液体所占的体积引入的实验误差,
故答案为:为避免加入硫酸时,液体所占的体积引入的实验误差.
点评 本题考查气体摩尔体积的测定实验,为高频考点,把握实验装置的作用、实验技能为解答关键,侧重分析与实验能力的考查,注意测定原理,题目难度不大.


科目:高中化学 来源: 题型:推断题
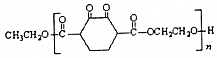 )是人造棉的主要成分之一,合成线路如图:
)是人造棉的主要成分之一,合成线路如图: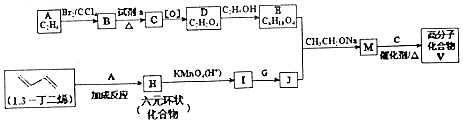
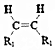 $\stackrel{KMnO_{4}/H+}{→}$2R1COOH
$\stackrel{KMnO_{4}/H+}{→}$2R1COOH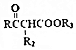 +R1OH
+R1OH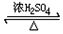 CH3CH2OOC-COOCH2CH3+2H2O.
CH3CH2OOC-COOCH2CH3+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
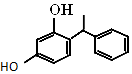 杨树生长迅速,高大挺拔,树冠有昂扬之势.其体内有一种有机物,结构如图所示.下列说法错误的是( )
杨树生长迅速,高大挺拔,树冠有昂扬之势.其体内有一种有机物,结构如图所示.下列说法错误的是( )| A. | 该有机物属于烃的衍生物 | |
| B. | 分子式为C14H14O2 | |
| C. | 1 mol该物质与溴水反应时最多能消耗2 mol的Br2 | |
| D. | 该有机物能与Na2CO3溶液反应,且生成的气体能使澄清石灰水变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,78g苯的碳碳双键数目为3NA | |
| B. | 1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价健数均为4NA | |
| C. | 500mL2mol/LNH4NO3溶液中,含有氮原子数目为2NA | |
| D. | 电解精炼铜时,若阳极质量减少32g,则阴极转移的电子数效目一定为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y4X10分子中,极性键和非极性键的个数比为10:4 | |
| B. | Z和W形成的多种化合物中只有一种能与水反应 | |
| C. | 25℃时,Z、W、X按原子个数比2:3:4形成的化合物的水溶液的pH=7 | |
| D. | 25℃时,等浓度的Z和Q的最高价氧化物对应水化物的水溶液中,水电离的c(H+)相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 向浓度均为1×10-4 mol/L的KCl和K2CrO4混合液中逐滴加入1×10-3 mol/LAgNO3溶液,CrO42-先沉淀(10-5 mol/L是否太小?这个浓度一般都认为沉淀完全了) | |
| B. | H2CO3、HCO3-、CH3COO-、ClO-在溶液中可以大量共存 | |
| C. | 相同浓度的CH3COONa和NaClO混合溶液,各离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+) | |
| D. | 碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O═HCO3-+Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com