
【化学–选修5:有机化学基础】(15分)
我国湖南、广西等地盛产的山苍子油中柠檬醛含量很高,质量分数可达到60%-90%,柠檬醛也可以利用异戊二烯为原料人工合成,柠檬醛又可用来合成紫罗兰酮等香精香料,其合成路线如下:
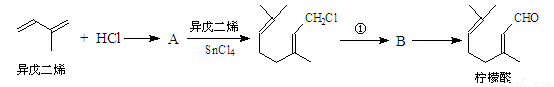
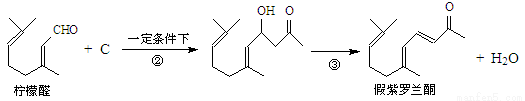
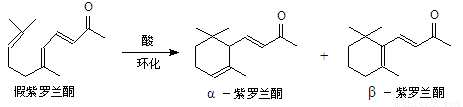
已知:①
②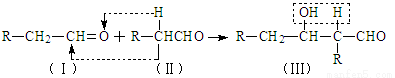
③同一碳原子连有两个双键结构不稳定。
试根据上述转化关系回答下列问题:
(1)写出A的结构简式 ,C的结构简式 。
(2)①对应的反应条件是 ,反应③的反应类型是 。
(3)写出B转化为柠檬醛的化学方程式 。
(4)根据反应②的反应机理写出CH3CHO与足量的HCHO反应产物的结构简式:
。
(5)检验柠檬醛中含有碳碳双键的实验方法是: 。

 (6)α-紫罗兰酮、β-紫罗兰酮有很多同分异构体,则满足下列条件的同分异构体有 种。
(6)α-紫罗兰酮、β-紫罗兰酮有很多同分异构体,则满足下列条件的同分异构体有 种。
①含有一个苯环 ②属于醇类且不能发生催化氧化反应
③核磁共振氢谱显示有5个峰
(15分)(1)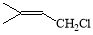 (2分)
(2分) 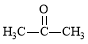 (2分)
(2分)
(2)NaOH的水溶液,加热 (2分) 消去反应 (1分)
(3)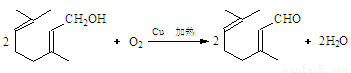 (2分)
(2分)
 (4)
(4) (2分)
(2分)
(5)向盛有少量溴的CCl4溶液的试管中滴加柠檬醛,边滴边振荡,若溶液变为无色则可证明(或:取少量柠檬醛与足量银氨溶液混合并置于热水浴中加热,充分反应后,取少量清液置于另一试管中,并滴加高锰酸钾酸性溶液,充分振荡,若高锰酸钾溶液褪色,则证明柠檬醛分子结构中有碳碳双键。) (2分)
(6)2 (2分)
【解析】
试题分析:(1)由A与异戊二烯发生反应生成的产物的结构简式判断,A的结构简式为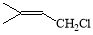 ;由柠檬醛与C的反应产物判断产物的右侧结构为C的结构,所以C是
;由柠檬醛与C的反应产物判断产物的右侧结构为C的结构,所以C是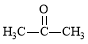 ;
;
(2)反应①应是卤代烃的水解反应,得醇再被氧化得柠檬醛,所以①对应的反应条件是NaOH的水溶液,加热 ;比较反应③前后的物质的结构,少了羟基,多了碳碳双键,判断反应③发生了消去反应;
(3)B生成柠檬醛发生的是氧化反应,化学方程式为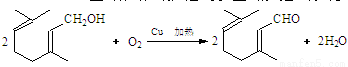 ;
;
(4)乙醛分子中的甲基上的3个H原子均与甲醛的羰基结合,生成羟醛结构的物质,所以最终得到的产物的结构简式为
(5)柠檬醛分子中存在碳碳双键和醛基,所以检验碳碳双键的存在需要注意区别二者的共同性质:都能使酸性高锰酸钾溶液褪色,所以选择溴的四氯化碳溶液,具体操作是向盛有少量溴的CCl4溶液的试管中滴加柠檬醛,边滴边振荡,若溶液变为无色则可证明;若选用酸性高锰酸钾溶液,则排除醛基的干扰后,再检验;
(6)α-紫罗兰酮、β-紫罗兰酮的分子式为C13H20O,利用不饱和度的计算,其不饱和度是4,所以同分异构体分子中除含苯环外无其他不饱和结构,属于醇类但不能发生催化氧化,说明取代基中存在类似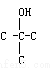 结构,且该分子中有5种氢原子,所以取代基具有对称结构,取代基共有7个C原子,所以应是2个取代基且是对位或是5个取代基,所以符合题意得共有2种同分异构体。
结构,且该分子中有5种氢原子,所以取代基具有对称结构,取代基共有7个C原子,所以应是2个取代基且是对位或是5个取代基,所以符合题意得共有2种同分异构体。
考点:考查有机物的推断,结构简式、化学方程式的判断与书写,官能团的检验,同分异构体的判断


科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:选择题
以下说法正确的是( )
A.不能自发进行的反应属于吸热反应
B.化学键断裂时吸收的能量大于化学键形成时放出的能量的反应属于放热反应
C.升高反应的温度,活化分子百分数增加,分子间有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应速率增大,但不改变反应所需的活化能
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉市高三四月调考理综化学试卷(解析版) 题型:简答题
(13分)某种电池的正极材料,可通过下列方法制得:
①称取一定量的固体铁氧体磁性材料溶于过量盐酸,接着先后加入双氧水和氢氧化钠溶液,静置24 h,过滤
②将沉淀加入反应瓶中,加入过量的氢氟酸溶液,80'c恒温加热24 ha
③蒸发多余氢氟酸和水,得淡红色FeF3凝胶
④在干燥箱中,以1000C预处理6 h,最后掺入铁氧体磁性材料混合研磨制得正极材料
(1)加入双氧水的作用是___(用离子方程式表示)
(2)步骤②的反应瓶材质可能是___(填序号)
A.玻璃 B.陶瓷 C.聚四氟乙烯
(3)加氢氟酸反生反应的化学方程式为____
(4)从安全的角度考虑,在实验室里制三氟化铁时应在____中进行
(5)三氟化铁与Li在固体电解质铁氧体中发生置换反应,产生的电流可供电脑使用,该电池反
应的化学方程式为____
(6)取上述铁氧体样品溶于足量盐酸,在通入标准状况下672 mL C12, Fe2+恰好被完全氧化成
Fe3十,然后把溶液蒸干,灼烧至恒重得9.6 g固体,则该铁氧体的化学式为____。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
A.这四种离子的电子层结构相同,因而离子的性质也就相同
B.原子序数:b>a>c>d
C.最高价氧化物对应水化物的碱性:B>A
D.气态氢化物的稳定性:D>C
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
A.在自然界中只以化合态的形式存在B.单质常用作半导体材料和光导纤维
C.最高价氧化物不与酸反应D.气态氢化物比甲烷稳定
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省宜昌市高三5月模拟理综化学试卷(解析版) 题型:实验题
(14分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:
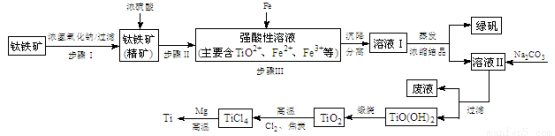
已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度与pH关系如图,

TiO(OH)2溶度积Ksp=1×10-29
①步骤Ⅲ加入铁屑原因 是 。
② TiO2+水解的离子方程式为 。
向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH= 时,TiO(OH)2已沉淀完全。
(3)TiCl4→Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
| TiCl4 | Mg | MgCl2 | Ti |
熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
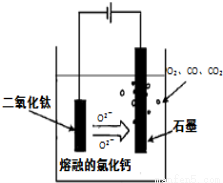
(4)电解TiO2制备钛的方法如图所示。该方法由于具备生产过程简化、生产成本低、产品质量高、环境友好等诸多优点而引人注目。已知TiO2熔融状态下不发生电离,电解时阴极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省宜昌市高三5月模拟理综化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列有关说法中不正确的是
A.航天服材质是由碳化硅/陶瓷和碳纤维等复合而成,它是一种新型无机非金属材料
B. 是放射性警示的标志
是放射性警示的标志
C.雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同
D.煤的主要成分为单质碳、苯、二甲苯等,因而可通过煤的干馏将它们分离
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省大冶市春季期末考试高二化学试卷(解析版) 题型:选择题
辨析以下的说法:①l6O与 l8O的转化可以通过化学反应实现;②灼烧钠的化合物时火焰呈黄色,那是发生了化学反应;③碱性氧化物一定是金属氧化物;④只由一种元素组成的物质一定是纯净物;⑤石墨与金刚石的转化是化学变化;⑥ 5424Cr为铬的一种核素,其核外电子数为30. 上述说法中正确的是
A.①④⑤ B.①③④ C.③⑤ D.②③⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014海口市第二学期高二化学期中考试(B卷)试卷(解析版) 题型:选择题
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
A.蒸馏常用于分离提纯液态有机混合物
B.燃烧法是研究确定有机物成分的有效方法
C.核磁共振氢谱通常用于分析有机物的相对分子质量
D.对有机物分子红外光谱图的研究有助于确定有机物分子中的基团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com