
【题目】下列各原子或离子的电子排布式错误的是( )
A. K+1s22s22p63s23p6
B. F 1s22s22p5
C. S2-1s22s22p63s23p4
D. Ar 1s22s22p63s23p6
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏伽德罗常数,下列说法正确的是( )
A.常温常压32g O2 含2NA个原子
B.标准状况下11.2L H2O 含有的原子数目为1.5NA
C.1mol的Cl﹣ 含有NA个电子
D.0.5mol/L的NaCl 溶液中Cl﹣的个数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中可逆反应A2(g)+3B2(g)═2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( ) 
A.加入催化剂可以使状态d变为状态b
B.若T1>T2 , 则逆反应一定是放热反应
C.达到平衡时A2的转化率大小为:b>a>c
D.在T2和n(A2)不变时达到平衡,AB3的物质的量大小为:c>b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素的元素序数依次增大.A的原子序数等于周期数;B的最外层电子数是次外层电子数的2倍,D的L层有两对成对电子;E+的核外有三个电子层,且都处于全满状态.试回答下列问题:
(1)基态E原子核外电子的排布式为
(2)A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为 , 阴离子的中心原子轨道采用杂化.
(3)B、C、D三种元素的第一电离能有大到小的顺序是(填元素符号)
(4)E(CA3)42+离子的颜色是;含有化学键类型是;该配离子中心离子的配位数为
(5)D、E能形成两种晶体,其晶胞分别如甲、乙两图.在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质.该化学反应方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如图所示),下列有关说法正确的是( ) 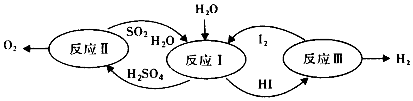
A.设计该循环是为了制取能源气体O2
B.整个循环过程中产生1mol O2的同时产生1molH2
C.图中反应Ⅰ,Ⅱ,Ⅲ均可在常温常压下进行
D.图中反应Ⅰ,Ⅱ,Ⅲ均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,a L气体X2和b L气体Y2恰好完全反应生成c L气体Z,若2a=6b=3c,则Z的化学式为
A. XY2 B. X3Y C. X2Y D. XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
选项 | A | B | C | D |
a | Na | Al | Fe | Cu |
b | NaOH | Al2O3 | FeCl3 | CuSO4 |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
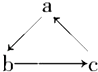
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是对某水溶液进行离子检验的方法和结论,其中不正确的是( )
A.先加入BaCl2溶液,产生了白色沉淀,再加入足量的HCl溶液,沉淀不溶解,溶液中一定含有大量SO ![]()
B.加入足量的CaCl2溶液,产生了白色沉淀,加入盐酸可以产生无色且能使澄清石灰水变浑浊的气体,则该溶液不一定含有大量的CO ![]()
C.加入足量浓 NaOH溶液加热,产生了带有强烈刺激性气味的能使湿润的红色石蕊试纸变蓝的气体,溶液中一定含有大量的NH ![]()
D.先加适量的硝酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com