
| A. | H2O的沸点比较高,是由于水分子间存在氢键的原因 | |
| B. | 除稀有气体外的非金属元素都能生成不同价态的含氧酸 | |
| C. | 若ⅡA族某元素的原子序数为m,则同周期ⅢA族元素的原子序数可能为m+11 | |
| D. | 由于分子间作用力比化学键弱得多,所以干冰升华容易,而CO2气体分解却不易 |
分析 A.氢键的存在使物质的熔沸点升高;
B.非金属元素中F和O元素无正价;
C.在第四周期和第五周期中,同周期ⅢA元素的原子序数比ⅡA原子序数多11;
D.分子间作用力的强度比化学键要弱得多.
解答 解:A.氢键的存在使物质的熔沸点升高,所以H2O的沸点比较高,故A正确;
B.非金属元素中F和O元素的非金属性强,无正价,故B错误;
C.在第四周期和第五周期中,同周期ⅢA元素的原子序数比ⅡA原子序数多11,故C正确;
D.干冰升华时只破坏分子间作用力,没有发生化学变化,则不破坏共价键,而分解破坏共价键,所以干冰升华容易,而CO2气体分解却不易,故D正确.
故选B.
点评 本题考查不同晶体的结构以及原子的构成等知识,为高考常见题型和高频考点,侧重于学生的分析能力和基本概念的综合理解和运用的考查,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学变化都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化都是化学变化 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

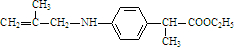 .
.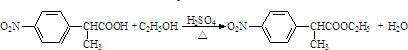 .
.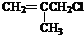 有相同官能团的同分异构体有10种.(要求考虑顺反异构)
有相同官能团的同分异构体有10种.(要求考虑顺反异构)查看答案和解析>>
科目:高中化学 来源: 题型:解答题

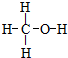 .
.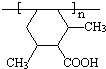 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成中含碳氢原子个数比为1:2 | |
| B. | 能与溴发生加成反应而使溴水褪色,还能使酸性KMnO4溶液褪色 | |
| C. | 在空气中燃烧能产生黑烟 | |
| D. | 完全燃烧生成等物质的量的CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.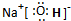 ,这种化合物中所含的化学键类型有离子键、共价键.
,这种化合物中所含的化学键类型有离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K[Ag(CN)2]、[Cu(NH3)4]SO4 | B. | [Ni(NH3)4]Cl2、[Ag(NH3)2]Cl | ||
| C. | [Ag(NH3)2]Cl、[Cu(NH3)2]Cl2 | D. | [Ni(NH3)4]Cl2、[Cu(NH3)4]SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com