
| A、氢氧化钠 | B、氧化钙 |
| C、碳酸钠 | D、碳酸钙 |


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
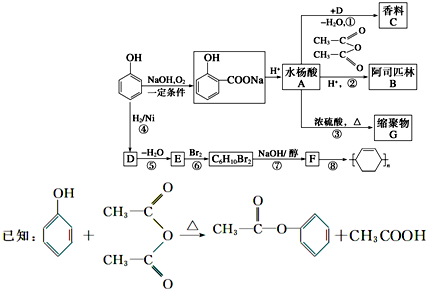
查看答案和解析>>
科目:高中化学 来源: 题型:
| O2 |
| 催化剂/△ |
| H2O |
| NaOH |
| 盐酸 |
| 盐酸 |
| 电解 |
| O2 |
| △ |
| CO2 |
| A、②④ | B、③④ | C、①④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 理由 | 结论 |
| A | 与盐酸反应时,相同物质的量的原子失去电子的数目:Al>Na | 还原性:Al>Na |
| B | 室温时,相同物质的量浓度溶液的pH:AlCl3<MgCl2 | 碱性:Mg(OH)2>Al(OH)3 |
| C | 相同数目的分子可电离的H+数:H2SO4>HClO4 | 酸性:H2SO4>HClO4 |
| D | 用饱和NaHCO3溶液可以除去CO2 中含有的少量SO2 | 非金属性:S>C |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
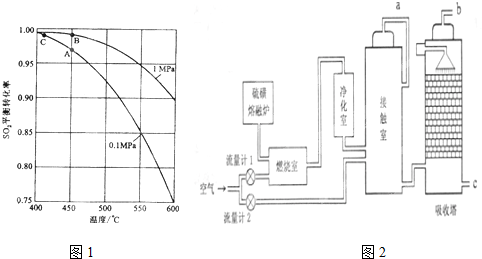
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
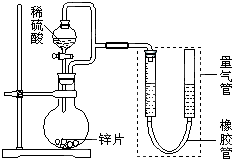 某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.据此回答下列问题:
某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.据此回答下列问题:| 序号 | V(H2SO4)/mL | c(H2SO4)/mol?L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com