
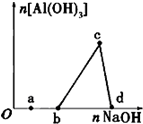
 一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:K+、Ag+、Ca2+、NO3- |
| B、b点对应的溶液中:K+、NH4+、CO32-、SO42- |
| C、c点对应的溶液中:Na+、Fe3+、SO42-、HCO3- |
| D、d点对应的溶液中:Na+、S2-、SO42-、Cl- |


科目:高中化学 来源: 题型:
| A、盐酸中加入碳酸钙:CO32-+2H+═H2O+CO2↑ |
| B、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学习小组利用中和反应原理和DIS系统测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点.实验步骤如下:
某学习小组利用中和反应原理和DIS系统测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点.实验步骤如下:+ 4 |
+ 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50 mL酸式滴定管;甲基橙 |
| B、50 mL碱式滴定管;酚酞 |
| C、50 mL量筒;石蕊 |
| D、50 mL酸式滴定管;不用指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 6
6
查看答案和解析>>
科目:高中化学 来源: 题型:
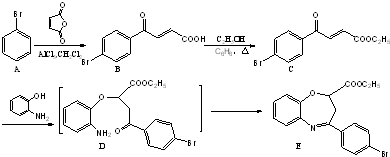
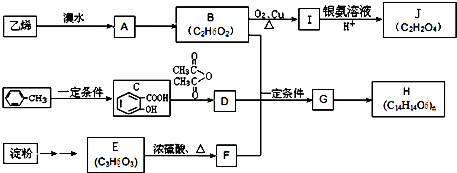
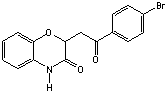 和一种常见的有机物F,F的结构简式为
和一种常见的有机物F,F的结构简式为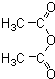
| H2O |
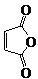 俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.
俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.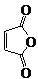 为原料制备化合物
为原料制备化合物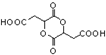 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:| 浓H2SO4 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
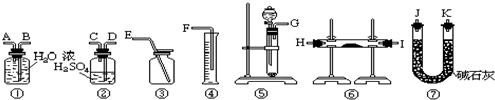
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管号 | 加入试剂 | 实验现象 | 离子方程式 |
| 1号 | 稀硫酸、H2O2、淀粉液 | 溶液立刻由褐色变成蓝色 | (1) |
| 2号 甲 | 新制的饱和氯水、1%淀粉液 | (2) | 2I-+Cl2=I2+2Cl- |
| 2号 乙 | 新制的饱和氯水、CCl4 | (3) | |
| 3号 | 食用碘盐、稀硫酸、1%淀粉液 | 溶液立刻由无色变成蓝色 | (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com