
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②HNO3 | ③NaOH ④KOH | ⑤Na2SO4 ⑥K2SO4 | ⑦SO2 ⑧SO3 | ⑨NH3 |
分析 (1)水溶液中电离出的阳离子全部是氢离子的化合物为酸,可以形成无氧酸、也可以形成含氧酸;
(2)⑦转化为⑧的反应是二氧化硫被氧气氧化生成三氧化硫;
(3)Cu和①的浓溶液加热反应生成硫酸铜、二氧化硫和水;
(4)利用氢氧化钙和氯化铵固体加热制备氨气,氨气是碱性气体可以利用湿润的红色石蕊试纸检验.
解答 解:(1)C、S、N元素中形成含氧酸的是S元素形成的碳酸、亚硫酸、硝酸等,
故答案为:HNO3;
(2)⑦转化为⑧的反应是二氧化硫被氧气氧化生成三氧化硫,反应的化学方程式为:2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3,
故答案为:2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3;
(3)Cu和①的浓溶液加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)═Cu SO4 +SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)═Cu SO4 +SO2↑+2H2O;
(4)实验室制备氨气是利用氢氧化钙和氯化铵固体加热反应生成,检验氨气存在的方法是:用湿润的红色石蕊试纸放于试管口,试纸变蓝,
故答案为:NH4Cl;Ca(OH)2;用湿润的红色石蕊试纸放于试管口,试纸变蓝;
点评 本题考查了物质分类、物质组成、物质性质、化学方程式书写等,主要是物质性质和气体制备、检验的分析应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改燃煤为燃气,可以减少废气中SO2等有害物质的排放量天气的一种措施 | |
| B. | 84 消毒液的有效成分是 NaClO | |
| C. | 含有食品添加剂的食物对人体健康不一定有益 | |
| D. | 金属防护中:牺牲阳极的阴极保护法利用的是电解原理,外加电流的阴极保护法利用的 是原电池原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b | |
| B. | 混合溶液的pH=7 | |
| C. | 混合溶液中c(H+)=$\sqrt{Kw}$ mol?L-1 | |
| D. | 向反应后的混合液中滴加石蕊试液后呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:1 | C. | 1:2 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
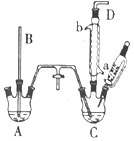 氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$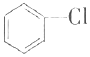 +HCl
+HCl查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 molNa2O2与足量的CO2充分反应转移的电子数为0.2NA | |
| B. | 常温常压下,18g H2O 所含的中子数为8NA | |
| C. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移 | |
| D. | 将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、NO3-、CO32- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Na+、Ag+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热氯化铁溶液的颜色变深 | |
| B. | NaHCO3做发酵粉时加入柠檬酸后效果更好 | |
| C. | 0.1 mol/L AlCl3溶液中c(Al3+)<0.1 mol/L | |
| D. | 常温下,CaCO3的饱和溶液pH约为9.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com