
 计算1.92g铜物质的量,铜屑投入HNO3和H2SO4的混合溶液中发生的反应:3Cu+8H++2NO3-=3Cu2++2NO+4H2O,结合铜、硝酸根、氢离子的物质的量根据离子方程式进行过量计算,再根据不足的物质计算铜离子的物质的量,结合c=
计算1.92g铜物质的量,铜屑投入HNO3和H2SO4的混合溶液中发生的反应:3Cu+8H++2NO3-=3Cu2++2NO+4H2O,结合铜、硝酸根、氢离子的物质的量根据离子方程式进行过量计算,再根据不足的物质计算铜离子的物质的量,结合c= 计算铜离子浓度.
计算铜离子浓度.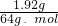 =0.03mol,
=0.03mol,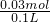 =0.3mol/L
=0.3mol/L

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省髙三第一次诊断性考试化学试卷 题型:选择题
在某100mL混合酸中,HNO3物质的量浓度为0.4mol/L,H2SO4物质的量浓度为0.2mol/L。向其中加入1.92克铜粉微热,待充分反应后,溶液中的Cu2+物质的量浓度为( )
A.0.15mol/L B.0.3mol/L C.0.225mol/L D.无法计算
查看答案和解析>>
科目:高中化学 来源:2014届四川省高一下学期2月学业检测化学试卷 题型:选择题
在某100mL混合酸中,HNO3的物质的量浓度为0.4mol/ L,H2SO4的物质的量浓度为0.2mol/L,向其中加入2.56g铜粉微热,待充分反应后,溶液中Cu2+
的物质的量浓度为( )
A.0.15mol/L B. 0.3mol/L C. 0.25mol/L D. 无法计算
查看答案和解析>>
科目:高中化学 来源:2006-2007学年山东省聊城市高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com