
已知Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH<0;则下列叙述不正确的是( )
| A.该反应的ΔH值与反应物用量无关 |
| B.该反应的化学能可以转化为电能 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量 |
科目:高中化学 来源: 题型:单选题
下列说法或表示方法正确的是
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由“C(石墨)=C(金刚石) ΔH=1.9kJ/mol”可知,金刚石比石墨稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,若将含1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=—285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学与生活、生产息息相关,下列说法不正确的是
| A.煤、石油、天然气属于化石能源,太阳能、氢能、风能、地热能、海洋能属于新能源 |
| B.测试和调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义 |
| C.利用盐类的水解反应可以制备胶体对饮用水进行净化,也可以获得纳米材料 |
| D.通常条件下能够自发进行的反应必须具备△H和△S均小于零 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是:
A.在100 ℃、101 kPa条件下,1mol液态水气化时需要吸收40.69 kJ的热量,则H2O(g) H2O(l) 的ΔH = +40.69 kJ·mol-1 H2O(l) 的ΔH = +40.69 kJ·mol-1 |
| B.已知CH4 (g)+2O2(g)=CO2(g)+2H2O(l);△H=-802.33kJ/mol,则CH4的燃烧热为802.33 kJ |
C.H2(g)+Br2(g)=2HBr(g)△H=-72kJ·mol-1其它相关数据如下表: 则表中a为230 |
| D.已知S (g)+O2(g)=SO2(s);△H1,S (g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相同的。
已知:①H2O(g)=H2O(l) ΔH1=-Q1 kJ/mol
②C2H5OH(g)=C2H5OH(l) ΔH2=-Q2 kJ/mol
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH3=-Q3 kJ/mol
若使23 g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)( )
| A.Q1+Q2+Q3 | B.1.5Q1-0.5Q2+0.5Q3 |
| C.0.5Q1-1.5Q2+0.5Q3 | D.0.5(Q1+Q2+Q3) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,下列说法不正确的是( )
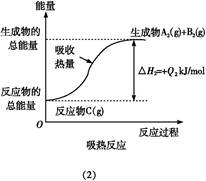
A.反应过程(1)的热化学方程式为A2(g)+B2(g) C(g)ΔH1=-Q1 kJ/mol C(g)ΔH1=-Q1 kJ/mol |
B.反应过程(2)的热化学方程式为C(g) A2(g)+B2(g)ΔH2=+Q2 kJ/mol A2(g)+B2(g)ΔH2=+Q2 kJ/mol |
| C.Q1与Q2的关系:Q1>Q2 |
| D.ΔH2>ΔH1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业生产水煤气的反应为:C(s)+ H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ·mol-1,下列判断正确的是( )。
| A.反应物能量总和大于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(l) ΔH=-131.4 kJ·mol-1 |
| C.水煤气反应中生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,图像表示某一反应过程中的能量变化曲线。下列说法中不正确的是( )
| A.由图可知,该反应为放热反应 |
| B.该反应的焓变为ΔH=-(E2-E1) |
| C.曲线b相对曲线a来说,改变的条件只能是使用了催化剂 |
| D.该反应的发生条件一定是加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com