
| A. | 反应中消耗O2 56 g | |
| B. | 所得产物中各物质的物质的量相等 | |
| C. | 若将产物通过碱石灰,不能被完全吸收 | |
| D. | 若将产物通过浓硫酸,充分吸收后,浓硫酸增重36g |
分析 由质量守恒可知氧气的质量为72g-1mol×16g/mol=56g,则氧气的物质的量为$\frac{56g}{32g/mol}$=1.75mol,1mol甲烷完全燃烧生成二氧化碳与水消耗氧气的物质的量为(1+$\frac{4}{4}$)mol=2mol>1.75mol,若生成CO与水,根据原子守恒可知消耗氧气的物质的量为$\frac{1mol+2mol}{2}$=1.5mol<1.75mol,故甲烷燃烧生成二氧化碳、一氧化碳与水,根据H原子守恒可知生成水为2mol,二氧化碳、一氧化碳总物质的量为1mol,以此来解答.
解答 解:A.由质量守恒可知氧气的质量为72g-1mol×16g/mol=56g,故A正确;
B.由原子守恒可知,生成水为2mol,二氧化碳、一氧化碳总物质的量为1mol,故B错误;
C.CO与碱石灰不反应,则产物通过碱石灰,不能被完全吸收,故C正确;
D.生成水为2mol×18g/mol=36g,则产物通过浓硫酸,充分吸收后,浓硫酸增重36g,故D正确;
故选B.
点评 本题考查化学反应的计算,为高频考点,把握完全燃烧消耗的氧气及产物的判断为解答的关键,侧重分析与计算能力的考查,注意质量守恒及原子守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
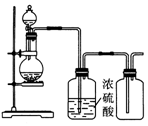
| A. | 亚硫酸钠固体与硫酸反应制二氧化硫 | |
| B. | 铜与稀硝酸反应制一氧化氮 | |
| C. | 氯化铵与氢氧化钙固体反应制氨气 | |
| D. | 锌和稀硫酸反应制氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,30 g乙烷气体中所含有的共价键数目为6NA | |
| B. | 常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA | |
| C. | 常温下,1 L pH=12的氨水溶液中含有NH4+数目为0.01NA | |
| D. | 1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 发生装置 | 收集装置 | 洗气装置 |
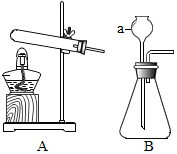 |  | 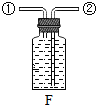 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
| 熔点/℃ | 872 | 275 | 394 | 446 |
| 在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
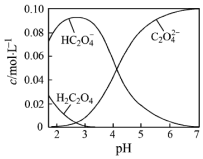 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定不正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定不正确的是( )| A. | pH=7的溶液中:c(Na+)>2c(C2O42-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | c(HC2O4-)=c(C2O42-)的点的坐标为(4.3,0.5),则Na2C2O4的水解平衡常数为Kh=1×10-9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羽绒服中的鸭绒和羽绒棉的主要成分都是蛋白质 | |
| B. | 在食品袋中放入装有生石灰和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 含氮、磷的污水是很好的肥料,可直接排放到自然界水体中用于灌溉庄稼 | |
| D. | 煤燃烧排放的废气中含大量CO2、SO2,是形成“硫酸型”酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2、MgO熔点高,可用于制作耐高温仪器 | |
| B. | 纤维素属于多糖类物质,但不能作人类的营养物质 | |
| C. | 硝酸铵属于氧化剂,严禁用可燃物(如纸袋)包装 | |
| D. | 天然气是可再生清洁能源,可用于工业制盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com