
(14分)水煤气是一种高效气体燃料,其主要成分是CO和H2,可用水蒸气通过炽热的炭制得:C
(s) + H2O(g) CO (g) +H2 (g) △H
=+131kJ•mol-1
CO (g) +H2 (g) △H
=+131kJ•mol-1
⑴T温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
|
容器 编号 |
c(H2O) /mol·L-1 |
c(CO) /mol·L-1 |
c(H2) /mol·L-1 |
v正、v逆比较 |
|
I |
0.06 |
0.60 |
0.10 |
v正=v逆 |
|
II |
0.06 |
0.50 |
0.40 |
① |
|
III |
0.12 |
0.40 |
0.80 |
v正<v逆 |
|
IV |
0.12 |
0.30 |
② |
v正=v逆 |
① ② 在T温度下该反应的化学平衡常数为
⑵另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0 mol水蒸气 (H2O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”)。
⑶在一定条件下用水煤气能合成甲醇:CO(g)+2H2(g) CH3OH(g) △H>0给合成甲醇反应体系中通入少量CO则平衡向
移动,减小压强则平衡向
移动,降低温度则平衡向
移动(填左,右,不)
CH3OH(g) △H>0给合成甲醇反应体系中通入少量CO则平衡向
移动,减小压强则平衡向
移动,降低温度则平衡向
移动(填左,右,不)
⑷熔融盐燃料电池具有高的发电效率,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,其中一极通入CO,另一极通入空气和CO2的混合气体。根据上述信息,该燃料电池:负极反应式为 ;正极反应式为 。
(5)已知在常温常压下:
①2CH3OH (l)+3O2 (g) == 2CO2 (g)+4H2O (g) ΔH1=-1 275.6 kJ·mol-1
②2CO (g)+O2 (g) == 2CO2 (g) ΔH2=-566.0 kJ·mol-1
③H2O (g) = H2O (l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________________
(1)①v正 < v逆 (1分) ②0.40 (1分) 1.0(1分)
(2)25%(1分) 不变(1分)
(3)右 左 左(各1分,共3分)
(4)2CO-4e-+2CO32 -=4CO2 (2分) O2 +4e-+2CO2=2CO32 -(2分)
(5)CH3OH(l)+O2(g) == CO(g)+2H2O(l) ΔH=-442.8 kJ·mol-1(2分)
【解析】(1)根据I可知,平衡常数为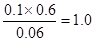 。II中
。II中 >1,所以反应向逆反应方向移动,即正反应速率小于逆反应速率。在IV中反应处于平衡状态,则
>1,所以反应向逆反应方向移动,即正反应速率小于逆反应速率。在IV中反应处于平衡状态,则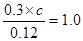 ,解得c=0.40mol/L。
,解得c=0.40mol/L。
(2)
C (s) + H2O(g) CO (g) +H2 (g)
CO (g) +H2 (g)
起始量(mol) 1 1 1
转化量(mol) x x x
平衡量(mol) 1-x x x
所以有1-x+x+x=1.25×1
解得x=0.25
所以转化率是0.25÷1×100%=25%
碳是固体,所以增加碳的质量是,平衡不移动。
(3)增加CO的浓度,平衡向正反应方向移动。因为反应是体积减小的、吸热的可逆反应,所以降低压强或降低温度平衡都向逆反应方向移动。
(4)原电池中负极失去电子,正极得到电子。又因为电解质是熔融盐,所以正负极的电极反应式为O2 +4e-+2CO2=2CO32 -、2CO-4e-+2CO32 -=4CO2 。
(5)根据盖斯定律可知,(①-②+③×4)÷2即得到CH3OH(l)+O2(g) == CO(g)+2H2O(l),所以ΔH=(-1 275.6 kJ·mol-1+566.0 kJ·mol-1-44.0 kJ·mol-1×4)÷2=-442.8 kJ·mol-1


科目:高中化学 来源: 题型:
 CO(g)+H2(g)△H=+131kJ?mol-1
CO(g)+H2(g)△H=+131kJ?mol-1| 容器 编号 |
c(H2O) /mol?L-1 |
c(CO) /mol?L-1 |
c(H2) /mol?L-1 |
v正、v逆比较 |
| I | 0.06 | 0.60 | 0.10 | v正=v逆 |
| II | 0.06 | 0.50 | 0.40 | ① |
| III | 0.12 | 0.40 | 0.80 | v正<v逆 |
| IV | 0.12 | 0.30 | ② | v正=v逆 |
 CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)
CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示) 2Cu+CO2
2Cu+CO2 2Cu+CO2
2Cu+CO2查看答案和解析>>
科目:高中化学 来源:2013届甘肃省甘谷一中高三上学期第一次检测考试理综化学试卷(带解析) 题型:填空题
(14分)水煤气是一种高效气体燃料,其主要成分是CO和H2,可用水蒸气通过炽热的炭制得:C (s) + H2O(g) CO (g) +H2 (g) △H=+131kJ?mol-1
CO (g) +H2 (g) △H=+131kJ?mol-1
⑴T温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器 编号 | c(H2O) /mol·L-1 | c(CO) /mol·L-1 | c(H2) /mol·L-1 | v正、v逆比较 |
| I | 0.06 | 0.60 | 0.10 | v正=v逆 |
| II | 0.06 | 0.50 | 0.40 | ① |
| III | 0.12 | 0.40 | 0.80 | v正<v逆 |
| IV | 0.12 | 0.30 | ② | v正=v逆 |
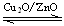 CH3OH(g) △H>0给合成甲醇反应体系中通入少量CO则平衡向 移动,减小压强则平衡向 移动,降低温度则平衡向 移动(填左,右,不)
CH3OH(g) △H>0给合成甲醇反应体系中通入少量CO则平衡向 移动,减小压强则平衡向 移动,降低温度则平衡向 移动(填左,右,不)查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
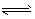 CO (g) +H2(g) △H=+131 kJ.mol-1。
CO (g) +H2(g) △H=+131 kJ.mol-1。 
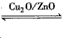 CH3OH(g),据研究,向合成甲醇的反应体系中通入少量CO,有利于维持催化剂Cu2O的量不变,原因是___ (用化学方程式表示)。
CH3OH(g),据研究,向合成甲醇的反应体系中通入少量CO,有利于维持催化剂Cu2O的量不变,原因是___ (用化学方程式表示)。 查看答案和解析>>
科目:高中化学 来源:2011年陕西师大附中高考化学三模试卷(解析版) 题型:解答题
 CO(g)+H2(g)△H=+131kJ?mol-1
CO(g)+H2(g)△H=+131kJ?mol-1| 容器 编号 | c(H2O) /mol?L-1 | c(CO) /mol?L-1 | c(H2) /mol?L-1 | v正、v逆比较 |
| I | 0.06 | 0.60 | 0.10 | v正=v逆 |
| II | 0.06 | 0.50 | 0.40 | ① |
| III | 0.12 | 0.40 | 0.80 | v正<v逆 |
| IV | 0.12 | 0.30 | ② | v正=v逆 |
 CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)______.
CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)______.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com