
如图所示,用a、b两惰性电极电解200mLCuSO4溶液,通电一段时间后,当a极的质量不再增加时,取出洗净干燥后,发现电极质量增加了6.4g。回答下列问题:
(1)标出电源的正负极。
(2)写出b极上发生的电极反应式以及溶液中总反应方程式。
(3)计算反应前CuSO4溶液的物质的量浓度以及反应后溶液中H+的浓度(不考虑溶液的体积变化)。
(4)反应完毕后加入_______可以使溶液与原溶液完全相同。

(1)c(负极),d(正极)
(2)4OH--4e-=2H2O+O2↑,2CuSO4+2H2O 2Cu+2H2SO4+O2↑
2Cu+2H2SO4+O2↑
(3)0.5mol?L-1,1mol?L-1 (4)8gCuO或12.4gCuCO3
 =0.1mol,所以原硫酸铜溶液的浓度为c(CuSO4)=
=0.1mol,所以原硫酸铜溶液的浓度为c(CuSO4)= =0.5mol?L-1。
=0.5mol?L-1。 2Cu + 2H2SO4 + O2↑, 显然
2Cu + 2H2SO4 + O2↑, 显然

科目:高中化学 来源: 题型:
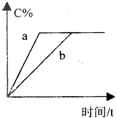
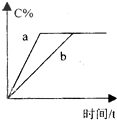 在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+2B(g)?3C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+2B(g)?3C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )查看答案和解析>>
科目:高中化学 来源: 题型:
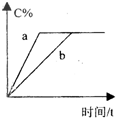 在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)?2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)?2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )查看答案和解析>>
科目:高中化学 来源:2013届甘肃省白银市恒学校高二上学期期末考试化学(理)试卷 题型:选择题
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)
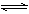 2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是
2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是
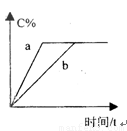
A.a的温度高于b
B.a使用了催化剂,而b未用
C.a的压强大于b
D.a的温度低于b
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a的温度高于b |
| B.a使用了催化剂,而b未用 |
| C.a的压强大于b |
| D.a的温度低于b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com