
| A. | 可加入酸性KMnO4溶液鉴别苯、乙醇和四氯化碳 | |
| B. | 碳酸钠溶液、蛋白质溶液均具有丁达尔效应 | |
| C. | 煤的干馏、石油的分馏、油脂的水解都是化学变化 | |
| D. | 蔗糖与稀硫酸溶液共热后加入银氨溶液,再水浴加热产生银镜,证明蔗糖水解产物中有葡萄糖 |
分析 A.苯与高锰酸钾分层后有机层在上层,乙醇与高锰酸钾发生氧化反应而褪色,四氯化碳与高锰酸钾分层后有机层在下层;
B.碳酸钠溶液不是胶体分散系;
C.石油的分馏与沸点有关,为物理变化;
D.蔗糖水解后,检验葡萄糖应在碱性条件下.
解答 解:A.苯与高锰酸钾分层后有机层在上层,乙醇与高锰酸钾发生氧化反应而褪色,四氯化碳与高锰酸钾分层后有机层在下层,现象不同,可鉴别,故A正确;
B.碳酸钠溶液不是胶体分散系,只有蛋白质溶液具有丁达尔效应,故B错误;
C.石油的分馏与沸点有关,为物理变化,而煤的干馏、油脂的水解都是化学变化,故C错误;
D.蔗糖水解后,检验葡萄糖应在碱性条件下,则水解后加碱至碱性,再加入银氨溶液,水浴加热,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
 常温下,用1L1mol•L-1Na2SO3溶液吸收SO2时,溶液pH随SO2的物质的量的变化如图所示,下列说法正确的是( )
常温下,用1L1mol•L-1Na2SO3溶液吸收SO2时,溶液pH随SO2的物质的量的变化如图所示,下列说法正确的是( )| A. | Na2SO3溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) | |
| B. | 当吸收液呈中性时,c(Na+)=c(HSO3-)+2c(SO32-) | |
| C. | M 点时溶液中:c(SO32-)>c(HSO3-) | |
| D. | 向N点的吸收液中加水可使溶液的pH由6.2升高到7.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 平衡时,各容器的压强:②=①=③ | B. | 平衡时,I2的浓度:②>①=③ | ||
| C. | 平衡时,I2的体积分数:②=①=③ | D. | 从反应开始到达平衡的时间:①>②=③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漏斗、烧杯、蒸发皿、酒精灯 | B. | 量筒、烧杯、试管夹、蒸发皿 | ||
| C. | 玻璃棒、蒸发皿、漏斗、集气瓶 | D. | 铁架台、天平、长颈漏斗、酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳 | B. | 钠 | C. | 硫 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 中的※C原子为手性碳原子;若一个碳原子上连着2个C=C(如
中的※C原子为手性碳原子;若一个碳原子上连着2个C=C(如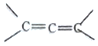 )时,极不稳定,不存在.现有某链烃C7H10的众多同分异构体中:
)时,极不稳定,不存在.现有某链烃C7H10的众多同分异构体中: ═CH-CH3
═CH-CH3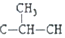 ═CH2
═CH2 -CH≡CH3
-CH≡CH3 ;
; .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com