
最近科学家在-100 ℃的低温下合成了一种烃X,其核磁共振氢谱表明该分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型。下列说法中错误的是( )
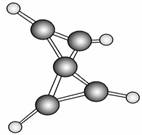 A.烃X的分子式为C5H4
A.烃X的分子式为C5H4
B.分子中碳原子的化学环境有2种
C.该有机物含有官能团
D.X分子中只有碳碳单键,没有碳碳双键
科目:高中化学 来源: 题型:
“辛烷值”用来表示汽油的质量,汽油中异辛烷爆震程度最小,将异辛烷爆震值标定为100,以下是异辛烷的球棍模型:
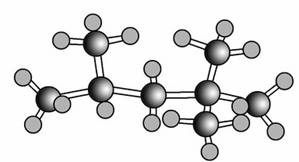
则利用系统命名法,异辛烷的系统名称为( )
A.1,1,3,3-四甲基丁烷
B.2,2,4-三甲基己烷
C.2,4,4-三甲基戊烷
D.2,2,4-三甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是 ( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列有关说法正确的是 ( )
A.蛋白质中只含C、H、O三种元素
B.糖类发生水解的最终产物都是葡萄糖
C.油脂的主要成分是高级脂肪酸甘油酯
D.糖类、油脂、蛋白质都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.氯化钙能吸水,不能吸收二氧化碳
B.相对分子质量为28的物质是乙烯
C.有机物分子式和实验式不可能相同
D.能使酸性高锰酸钾溶液褪色的有机物中含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定一种气态烃A的化学式,取一定量的A置于一密闭容器中燃烧,定性实验表明产物是CO2、CO 和水蒸气,学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的实验式。他们测得的有关数据如下(箭头表示气流方向,实验前系统内的空气已排尽):
甲:燃烧产物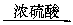 增重2.52 g
增重2.52 g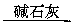 增重1.32 g
增重1.32 g 生成CO21.76 g
生成CO21.76 g
乙:燃烧产物 增重5.6 g
增重5.6 g 减重0.64 g
减重0.64 g 增重4.0 g
增重4.0 g
试回答:
(1)你认为能够求出A的实验式的方案是__________(填“甲”或“乙”),理由是_______________________________________________________________。
(2)根据你选择的方案,通过计算确定A的实验式为_____________________。
(3)若要确定A的化学式_____________(填“需要”或“不需要”)测定其他数据,其原因是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以NA表示阿伏加德罗常数,下列说法正确的是
A.在标准状况下,11.2 L己烷含有分子数为0.5NA
B.4.2 g乙烯和环丙烷的混合气体含有H原子数为0.6NA
C.甲基﹝-CH3﹞的电子总数为10NA
D.在常温常压下,2.24 L丁烷和2—甲基丙烷的混合气体所含分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
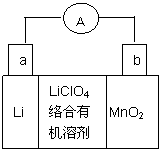
锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图
所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,
生成LiMnO2。回答下列问题:
 (1)a电极为__________极(填“正”或“负”)。
(1)a电极为__________极(填“正”或“负”)。
(2)电池正极反应式为_______________________。
(3)是否可用水代替电池中的混合有机溶_______
(填“是”或“否”),原因是___________________。
(4)MnO2与双氧水混合化学方程式为 ;
MnO2的作用是 。
(5)MnO2可与KOH和KClO3在高温条件下反应,生
成K2MnO4,反应的化学方程式为_________________________________________,
K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验。实验过程和记录如图所示(无关物质已经略去):
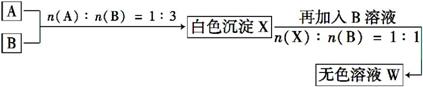

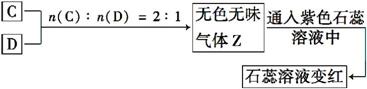
请回答:
(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为 、 。
(2)D溶液pH 7(填“大于”“小于”或“等于”),原因是(用离子方程式表示) 。
(3)等物质的量浓度的A、B、C、D溶液,pH由大到小的顺序是 (用化学式表示)。
(4)等物质的量浓度的C溶液与NH4Cl溶液相比较,c(N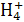 ):前者 后者(填“<”“>”或“=”)。
):前者 后者(填“<”“>”或“=”)。
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com