
下列分类,完全正确的是
| A | B | C | D | |
| 强电解质 | H2SO4 | NaCl | HClO | HNO3 |
| 弱电解质 | HF | NH3 | CaCO3 | H2CO3 |
| 非电解质 | Cl2 | CH3COOH | C2H5OH | SO2 |
科目:高中化学 来源: 题型:
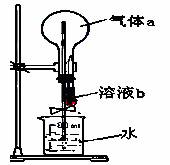
如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是( )
| 干燥气体a | 液体b | |
| A | NH3 | 水 |
| B | HCl | 水 |
| C | CO2 | NaOH溶液 |
| D | Cl2 | 饱和食盐水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可以证明可逆反应N2 + 3H2 2NH3已达到平衡状态的是 ( )
2NH3已达到平衡状态的是 ( )
①一个N≡N断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其它条件不变时,混合气体平均相对分子质量不再改变;④保持其它条件不变时,体系压强不再改变;⑤NH3、N2、H2的体积分数都不再改变;⑥恒温恒容时,混合气体的密度保持不变;⑦正反应速率v(H2) = 0.6 mol/(L·min),逆反应速率v(NH3) = 0.4 mol/(L·min)
A.全部 B.①③④⑤ C.②③④⑤⑦ D.③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
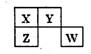
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中Y所处的周期序数与主族序数之和为8。下列说法错误的是
A.Z元素的氧化物对应水化物的酸性一定弱于W
B.四种元素中Z的原子半径和形成的离子半径均最大
C.X、Z、W中最简单气态氢化物稳定性最弱的是Z
D.X、Y、Z的原子均能与氢原子形成四原子分子
查看答案和解析>>
科目:高中化学 来源: 题型:
能源的开发和利用是当前科学研究的重要课题。
(1)利用二氧化铈(CeO2)在太阳能作用下前实现如下变废为宝的过程:
mCeO2 (m-x)CeO2
(m-x)CeO2 xCe+xO2
xCe+xO2
(m-x)CeO2 xCe+xH2O+xCO2
xCe+xH2O+xCO2 mCeO2+xH2+xCO
mCeO2+xH2+xCO
上述过程的总反应是 ,该反应将太阳能转化为 。
(2)CO、O2和KOH溶液构成的燃料电池的负极电极反应式为 。该电池反应可获得K2CO3溶液,某温度下0.5mol L-1。晦K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O
L-1。晦K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O HCO3-+OH-的平衡常熟Kh= 。
HCO3-+OH-的平衡常熟Kh= 。
(3)氯碱工业是高耗能产业,下列将电解池与燃料电池相组合的工艺可以节能30%以上。
①电解过程中发生反应的离子方程式是 ,阴极附近溶液PH (填“不变”、“升高”或“下降”)。
②如果粗盐中SO42-含量较高,精制过程需添加钡试剂除去SO42-,该钡试剂可选用下列试剂中的 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
现代工艺中更多使用BaCO3除SO42-,请写出发生反应的离子方程式 。
③图中氢氧化钠溶液的质量分数a% b%(填“>”、‘‘=”或“<”),,燃料电池中负极上发生的电极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于在密闭容器中进行的反应:N2+O2 2NO,下列不能加快该反应的反应速率的条件是
2NO,下列不能加快该反应的反应速率的条件是
A.体积增大到原的2倍 B.充入更多的NO C.缩小体积 D.升高温度

查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH=3的乙酸溶液,下列说法正确的是
A.c(H+)=c(CH3COO-)+c(OH-)
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH降低
D.与等体积pH=11的NaOH溶液混合后所得溶液中:c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是原子核电荷数不大于18的元素。若X、Y两元素化合物组成是YX3,已知X原子的最外层电子数为a+2,次外层电子数为a+3;Y原子的最外层电子数为b-3,次外层电子数为b。则a和b的值分别是( )
A、3,2 B、2,3 C、5,6 D、5,8
查看答案和解析>>
科目:高中化学 来源: 题型:
某饱和一元醛发生银镜反应时可以析出21.6g银,等量的醛完全燃烧可以产
生6.72LCO2(标况),则该醛为 ( )
A.乙醛 B.2-甲基丙醛 C.丙醛 D.丁醛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com